题目内容
某核素R具有微弱放射性,其原子核内中子数比质子数多43。有它组成的固体单质A,在一定条件下密度为6.88 g·cm-3。用X射线研究其固体表明:在边长为1.00×10-7 cm的立方体中含有20个原子。R在化学反应中常表现为+2价、+4价,在溶液中R2+稳定,而R4+具有氧化性,可将NO氧化为HNO3。氧化物R3O4的性质与Fe3O4有些类似。R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿的环境中易形成铁锈。R的单质及化合物在工业生产、医疗卫生、科学技术等各个领域都有很多用途,请完成下列问题:(1)R原子的摩尔质量。_____________________
(2)R原子的外围电子排布式。_____________________
(3)R元素处于周期表中的位置。_____________________?
(4)R4+加到FeCl2溶液中发生反应的离子方程式。_____________________?
(5)R3O4因具有氧化性,被大量用于油漆材料,涂在钢铁表面,有利于形成耐腐蚀的钝化层。R3O4与定量的HNO3反应,生成R的氧化物、R的硝酸盐和水三种物质。写出此反应的方程式。_______________________________________________________________
解析:M=m/20×6.02×1023 =ρV/20×6.02×1023
=[6.88 g·cm-3×(1.00×10-7 cm)3]/20×6.02×1023
=207 g·mol-1?
设质子数为x,x+x+43=207 则x=82根据周期表的排布规则,R元素处于周期表中的位置为第六周期ⅣA族。?
在溶液中R2+稳定,R4+具有氧化性,因此可与Fe2+发生氧化还原反应R4++2Fe2+![]() R2++2Fe3+?
R2++2Fe3+?
R3O4与定量的HNO3反应,生成R的氧化物、R的硝酸盐和水三种物质,在溶液中R2+稳定,因此可得方程式R3O4+4HNO3![]() RO2+2R(NO3)2 +2H2O。?
RO2+2R(NO3)2 +2H2O。?
答案:(1)207 g·mol-1?
(2)6s26p2
(3)第六周期ⅣA族?
(4)R4++2Fe2+![]() R2++2Fe3+?
R2++2Fe3+?
(5)R3O4+4HNO3![]() RO2+2R(NO3)2 +2H2O
RO2+2R(NO3)2 +2H2O

| |||||||||||||||||||
 ,用X射线研究其固体表明,在边长为1.00×
,用X射线研究其固体表明,在边长为1.00× 的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中
的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中 稳定,而
稳定,而 有强氧化性,可将NO氧化为
有强氧化性,可将NO氧化为 .氧化物
.氧化物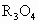 ,其性质与
,其性质与 有些类似.R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈.R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途.
有些类似.R的另一种质量数比R少2的同位素较为稳定,与铁可形成合金,在潮湿环境中易形成铁锈.R的单质及化合物在工农业生产、医疗卫生、科学技术等各个领域都有很多用途. 溶液中,是否会发生反应?
溶液中,是否会发生反应? 反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________.
反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为________.