题目内容
许多物质的氧化能力受溶液酸碱性的影响.高锰酸钾在不同条件下发生的还原反应如下:MnO4-+5e+8H+→Mn2++4H2O MnO4-+3e+2H2O→MnO2+4OH-
MnO4-+e→MnO42-(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H++2e→Mn2++2H2O
(1)MnO2 与稀盐酸不能制取氯气,其原因是______.
(2)将SO2通入KMnO4溶液中,发生还原反应的过程为______→______(用化学式或离子符号表示).
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列叙述正确的是______(选填编号).
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,其中K2SO4和S的物质的量之比为3:2.完成并配平该反应的化学方程式.
______KMnO4+______K2S+______→______K2MnO4+______K2SO4+______S↓+______
反应若生成5.44g单质硫,反应过程中转移电子的物质的量为______.
【答案】分析:(1)MnO2在溶液酸性较弱的环境中没有制取氯气的氧化能力;
(2)得电子化合价降低的微粒发生还原反应;
(3)同一化学反应中氧化剂的氧化性大于还原产物的氧化性;
(4)根据氧化还原反应中得失电子数相等配平方程式,并注意也要遵循原子守恒;根据硫单质和转移电子之间的关系式计算转移电子的物质的量.
解答:解:(1)二氧化锰有氧化性,但必须是MnO2在溶液酸性较强的环境中才有制取氯气的氧化能力,所以MnO2 与稀盐酸不能制取氯气,
故答案为:MnO2在溶液酸性较强的环境中才有制取氯气的氧化能力;
(2)二氧化硫含有还原性,酸性条件下,高锰酸根离子得电子生成二价锰离子,所以高锰酸根离子有强氧化性,所以还原反应的过程为MnO4-→Mn2+,
故答案为:MnO4-→Mn2+;
(3)同一化学反应中,氧化剂的氧化性大于氧化产物的氧化性,将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色,说明PbO2氧化二价锰离子生成高锰酸根离子,所以PbO2作氧化剂,高锰酸根离子是氧化产物,所以PbO2的氧化性大于高锰酸根离子,故选a;
(4)该反应中,高锰酸钾是氧化剂,一个高锰酸钾化学式得5个电子,硫化钾是还原剂,K2SO4和S的物质的量之比为3:2,所以硫化钾生成硫酸钾和硫单质失去的电子数是28个电子,所以得失电子的最小公倍数是140,所以高锰酸钾的计量数是25,硫化钾的计量数是5,其它元素根据原子个数相等配平,所以方程式为:28KMnO4+5K2S+24KOH=28K2MnO4+3K2SO4+3S↓+12H2O;
设转移电子的物质的量是xmol.
28KMnO4+5K2S+24KOH=28K2MnO4+3K2SO4+2S↓+12H2O 转移电子
2mol 140mol
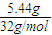 xmol
xmol
x=11.9,
故答案为:28;5;24KOH;28;3;2;12H2O;11.9mol.
点评:本题考查了有关物质的量的计算、氧化性和还原性的判断等知识点,难度不大,明确同一反应中氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性.
(2)得电子化合价降低的微粒发生还原反应;
(3)同一化学反应中氧化剂的氧化性大于还原产物的氧化性;
(4)根据氧化还原反应中得失电子数相等配平方程式,并注意也要遵循原子守恒;根据硫单质和转移电子之间的关系式计算转移电子的物质的量.
解答:解:(1)二氧化锰有氧化性,但必须是MnO2在溶液酸性较强的环境中才有制取氯气的氧化能力,所以MnO2 与稀盐酸不能制取氯气,
故答案为:MnO2在溶液酸性较强的环境中才有制取氯气的氧化能力;
(2)二氧化硫含有还原性,酸性条件下,高锰酸根离子得电子生成二价锰离子,所以高锰酸根离子有强氧化性,所以还原反应的过程为MnO4-→Mn2+,
故答案为:MnO4-→Mn2+;
(3)同一化学反应中,氧化剂的氧化性大于氧化产物的氧化性,将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色,说明PbO2氧化二价锰离子生成高锰酸根离子,所以PbO2作氧化剂,高锰酸根离子是氧化产物,所以PbO2的氧化性大于高锰酸根离子,故选a;
(4)该反应中,高锰酸钾是氧化剂,一个高锰酸钾化学式得5个电子,硫化钾是还原剂,K2SO4和S的物质的量之比为3:2,所以硫化钾生成硫酸钾和硫单质失去的电子数是28个电子,所以得失电子的最小公倍数是140,所以高锰酸钾的计量数是25,硫化钾的计量数是5,其它元素根据原子个数相等配平,所以方程式为:28KMnO4+5K2S+24KOH=28K2MnO4+3K2SO4+3S↓+12H2O;
设转移电子的物质的量是xmol.
28KMnO4+5K2S+24KOH=28K2MnO4+3K2SO4+2S↓+12H2O 转移电子
2mol 140mol
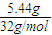 xmol
xmolx=11.9,
故答案为:28;5;24KOH;28;3;2;12H2O;11.9mol.
点评:本题考查了有关物质的量的计算、氧化性和还原性的判断等知识点,难度不大,明确同一反应中氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目