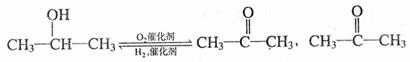题目内容
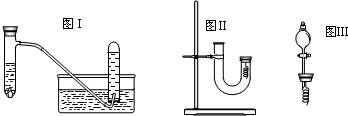
(11分)为证明有关物质的性质,某学生设计了如图所示的装置。当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛熄灭;关闭C 打开E时,则看到G中蜡烛燃得更亮。
(1)请判断各仪器中盛放的物质的化学式:
A ; B ;F 。
(2)用化学反应方程式表示上述有关反应(不包括蜡烛的燃烧):
,
,
.
(1)A .HCl B.CaCO3 F.Na2O2
(2)CaCO3+2HCl = CaCl2+H2O+CO2↑; 2Na2O2+2CO2 = 2Na2CO3+O2 ;2Na2O2+2 H2O = 4NaOH+O2
解析试题分析:D中蜡烛熄灭,说明试管中生成了二氧化碳气体,试管中发生的反应是实验室制取二氧化碳气体的反应;G中蜡烛燃烧更旺,说明G中生成了氧气,应是二氧化碳与过氧化钠发生反应,二氧化碳气体通过过氧化钠时气体未干燥,所以还有过氧化钠与水蒸气的反应。
(1)A、B、F分别为HCl、CaCO3、Na2O2。
(2)有关反应方程式为CaCO3+2HCl = CaCl2+H2O+CO2↑; 2Na2O2+2CO2 = 2Na2CO3+O2 ;2Na2O2+2 H2O = 4NaOH+O2↑。
考点:化学实验
点评:二氧化碳气体通过过氧化钠时没有用干燥剂干燥二氧化碳气体,所以二氧化碳气体中混有水蒸气,当然应该还有氯化氢与过氧化钠的反应。


(1)写出试管内溶液中发生反应的化学方程式______
(2)在实验过程中观察到试管内的溶液呈______色;收集气体的试管内的气体呈______色
(3)乙同学认为甲虽然收集到的气体是一氧化氮,但并不能说明反应中一定生成一氧化氮.他的理由是____________
有关化学方程式为:______
(4)丙同学釆用如图Ⅱ所示装置进行实验,证明了铜与稀硝酸反应生成一氧化氮.该同学的步骤如下表所示,请回答实验中的有关问题.
| 实验步骤 | 问题 |
| 1从U型管左端加入稀硝酸直至充满U型管右端 | ∥/ |
| 2用附有铜丝的胶塞塞住U型管右端,观察现象 | 现象是______ |
| 3待反应停止后打开胶塞,观察实验现象 | 现象是______ |
(6)丁同学用图Ⅲ所示装置代替图Ⅱ中U型管右端的附有铜丝的胶塞进行实验,待反应停止后将一氧化氮气体排入分液漏斗中,观察到的实验现象与丙同学实验的第______步骤的相同.丁同学要将一氧化氮气体排入分液漏斗中应进行的正确操作是①______②______③______
(7)实验结束后丁同学向分液漏斗中注入适量水并充分振荡,试写出发生的化学反应方程式______
(8)若将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L(不考虑NO2的反应),试回答:
①若铜与硝刚好反应完全,则原硝酸溶液的物质的量浓度为______
②将产生的气体全部释放后,向溶液中加入VmL amol?L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的物质的量浓度为______
③已知NO和NO2的混合气与足量氧气混合后能被水完全吸收成硝酸,则要使上述11.2L气体完全被水吸收成硝酸,理论上需消耗标准状况下的氧气______升.(保留两位小数);解题过程:______
2003年11月《环球时报》(美)报道,ACV浓缩饮料风靡全美,ACV具有解毒、降脂、减肥和止泻等多种疗效,其中苹果酸M(分子量134)是主要的活性物质,其化学成分及有关实验如下:
①含C35.82%(质量分数,下同),含H4.51%,其余为氧元素;
②各取1×10-3molM分别与足量NaHCO3反应放出CO244.8mL(标准状况,下同),与足量金属钠反应放出H233.6mL
③M分子中所有碳原子在同一链线上。
回答下列问题:
(1)M的化学式为: ,分子中含的官能团名称是 。
(2)已知M有多种同分异构体,试写出其中符合下述要求的结构简式(限写一种)。
1mol该有机物与足量金属钠反应生成1molH2: 。
|
(已知不能被O2氧化,但可与H2加成)
合成路线为:N→有机物A→有机物B→有机物C→M,其中B能发生银镜反应。
①有机物N的结构简式为 ;
②A转化为B的化学方程式为 。
③有机物C转化为M的反应类型为 。
(4)实验证明M分子间可形成具有水果香味的化合物,若该化合物分子中含有的环状结构,其结构简式可能为: 。