题目内容
(9分) 实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
(1)为了节约原料,硫酸和硝酸的物质的量之比最佳为____________;
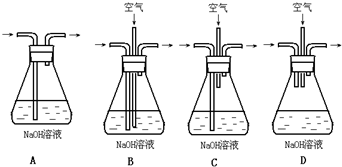
为了吸收该反应中产生的尾气,可选择的最佳装置是_______________。

(2)为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:以空气为氧化剂。将铜粉在仪器N中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,再通入空气或氧气,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH ,铁元素全部转化为Fe(OH)3沉淀(一般认为铁离子的浓度下降到10-5 mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
(已知:Ksp[Cu(OH)2]≈10-22, Ksp[Fe(OH)3]≈10-38)
请回答下列问题:
①方案1中的N仪器名称是 ______________。
②为了使铁元素全部沉淀,应调节pH至少为_________。
③方案2中甲物质可选用的是________________________。
A.CaO B.NaOH C.CuCO3 D.Cu2(OH)2CO3 E.Fe2(SO4)3
④反应中加入少量FeSO4可加速铜的氧化,用离子方程式解释其原因___________________________________________________。
【答案】

【解析】

练习册系列答案
相关题目