题目内容
(1)2012年世界青年奥运会将在南京举办.保护环境,人人有责.
①在处理产生的废水时,需先加入明矾,其作用是作______;后通入氯气或二氧化氯,其作用是作______.
②改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量.为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行______.
(2)我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出杰出贡献,荣获2010年度国家最高科学技术奖.
①汽车尾气(含有烃类、CO、SO2与NO等物质)治理的方法之一是在汽车的排气管上装一个用铂、钯合金作催化剂的催化转换器.它的特点是使CO与NO反应,生成无毒气体,并促使烃类充分燃烧及SO2的转化.写出CO与NO反应的化学方程式:______.
②钢铁是人们生活中常用的金属材料,也是一种合金.如图所示,钢铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)______.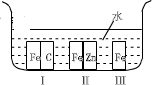
(3)经研究,光化学烟雾的有害物质中含有臭氧,其形成过程与二氧化氮有关,这个过程实际上包含了三个反应:
①NO2 NO+O、②2NO+O2=2NO2、③O2+O=O3.则总反应可表示为______,NO2在其中起了______作用.
NO+O、②2NO+O2=2NO2、③O2+O=O3.则总反应可表示为______,NO2在其中起了______作用.
解:(1)①明矾易水解生成氢氧化铝胶体,胶体具有吸附性,能吸附水中的悬浮物而净水,所以明矾常用作混凝剂,氯气和二氧化硫能杀菌消毒,故答案为:作混凝剂,消毒剂;
②化石燃料会产生大量的二氧化碳,还会产生二氧化硫,为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行脱硫,故答案为:脱硫处理;
(2)①一氧化氮和一氧化碳都有毒,在催化剂条件下,一氧化碳和一氧化氮反应生成无毒物质,根据元素守恒知,氮气和二氧化碳无毒,所以其生成物是氮气和二氧化碳,反应方程式为:2NO+2CO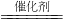 N2+2CO2,故答案为:2NO+2CO
N2+2CO2,故答案为:2NO+2CO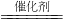 N2+2CO2;
N2+2CO2;
②I中碳和铁、电解质溶液构成原电池,碳作正极,铁作负极而加速被腐蚀,II中铁、锌和电解质溶液构成原电池,锌作负极,铁作正极而被保护,所以铁被腐蚀的速率由大到小的顺序是:Ⅰ>Ⅲ>Ⅱ,
故答案为:Ⅰ>Ⅲ>Ⅱ;
(3)将方程式①×2+②+③×2得总方程式为3O2═2O3,在方程式①二氧化氮是反应物,在方程式②中二氧化氮 生成物,在总反应方程式中没有二氧化氮,所以二氧化氮起催化剂作用,故答案为:3O2═2O3;催化剂.
分析:(1)①明矾水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性;氯气和二氧化氯常用作消毒剂;
②化石燃料会产生大量的二氧化碳,还会产生二氧化硫;
(2)①在催化剂条件下,一氧化碳和一氧化氮反应生成氮气和二氧化碳;
②作原电池负极的金属加速腐蚀,作原电池正极的金属被保护;
(3)将方程式①×2+②+③×2得总方程式,二氧化氮其催化剂作用.
点评:本题考查了环境污染及治理,难度不大,会运用化学知识解决生产生活问题,学以致用.
②化石燃料会产生大量的二氧化碳,还会产生二氧化硫,为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行脱硫,故答案为:脱硫处理;
(2)①一氧化氮和一氧化碳都有毒,在催化剂条件下,一氧化碳和一氧化氮反应生成无毒物质,根据元素守恒知,氮气和二氧化碳无毒,所以其生成物是氮气和二氧化碳,反应方程式为:2NO+2CO
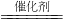 N2+2CO2,故答案为:2NO+2CO
N2+2CO2,故答案为:2NO+2CO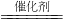 N2+2CO2;
N2+2CO2; ②I中碳和铁、电解质溶液构成原电池,碳作正极,铁作负极而加速被腐蚀,II中铁、锌和电解质溶液构成原电池,锌作负极,铁作正极而被保护,所以铁被腐蚀的速率由大到小的顺序是:Ⅰ>Ⅲ>Ⅱ,
故答案为:Ⅰ>Ⅲ>Ⅱ;
(3)将方程式①×2+②+③×2得总方程式为3O2═2O3,在方程式①二氧化氮是反应物,在方程式②中二氧化氮 生成物,在总反应方程式中没有二氧化氮,所以二氧化氮起催化剂作用,故答案为:3O2═2O3;催化剂.
分析:(1)①明矾水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性;氯气和二氧化氯常用作消毒剂;
②化石燃料会产生大量的二氧化碳,还会产生二氧化硫;
(2)①在催化剂条件下,一氧化碳和一氧化氮反应生成氮气和二氧化碳;
②作原电池负极的金属加速腐蚀,作原电池正极的金属被保护;
(3)将方程式①×2+②+③×2得总方程式,二氧化氮其催化剂作用.
点评:本题考查了环境污染及治理,难度不大,会运用化学知识解决生产生活问题,学以致用.

练习册系列答案
相关题目
 (1)下列常用物质:
(1)下列常用物质:
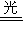 NO+O、②2NO+O2=2NO2、③O2+O=O3.则总反应可表示为 ,NO2在其中起了 作用.
NO+O、②2NO+O2=2NO2、③O2+O=O3.则总反应可表示为 ,NO2在其中起了 作用.