��Ŀ����
����Ŀ����ͼ�Ǵ�Ԫ�����ڱ��н�ȡ��һ��Ƭ�Σ�����X��Y��Z��W�����ڶ�����Ԫ�أ���ش��������⣮
��1����X����Ϊ�����е���Ҫ�ɷ�֮һ����W��ԭ�ӽṹʾ��ͼΪ ��
��2����Y��W��Z������������Ӧ��ˮ��������ΪһԪ�ᡢ��Ԫ�ᡢ��Ԫ�ᣬ������������εĺ�����������У������ֵĵ�������ȣ����������ӵ����ӷ������� ��
��3����Na��Y��Z�ĵ��ʷֱ�Ӧ��������Ħ��������ͬ�����ֻ��������Na��Y�γɵĻ�����ĵ���ʽΪ �� ������ѧ��������Ϊ ��
��4��YԪ����Ԫ�����ڱ��д��ڵ����У�д�����п��ܵ����������� ![]()
���𰸡�
��1��![]()
��2��SO42����PO43��
��3��![]() �����Ӽ������ۼ�
�����Ӽ������ۼ�
��4��15��16��17
���������⣺��1����X�ĵ���Ϊ��������Ҫ�ɷ�֮һ����X��NԪ�ء�W��ArԪ�أ�ArԪ�ص�ԭ�ӽṹʾ��ͼΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����2����Y��W��Z������������Ӧ��ˮ��������ΪһԪ�ᡢ��Ԫ�ᡢ��Ԫ�ᣬ��ֱ�ΪHNO3��H2SO4��H3PO4 �� ����SO42����PO43���ĵ�������ȣ����Դ��ǣ�SO42����PO43������3����Na��Y��Z�ĵ��ʷֱ�Ӧ����Ħ��������ͬ�����ֻ������ΪNa2O2��Na2S������Na2O2�ĵ���ʽΪ
����2����Y��W��Z������������Ӧ��ˮ��������ΪһԪ�ᡢ��Ԫ�ᡢ��Ԫ�ᣬ��ֱ�ΪHNO3��H2SO4��H3PO4 �� ����SO42����PO43���ĵ�������ȣ����Դ��ǣ�SO42����PO43������3����Na��Y��Z�ĵ��ʷֱ�Ӧ����Ħ��������ͬ�����ֻ������ΪNa2O2��Na2S������Na2O2�ĵ���ʽΪ ![]() �����������Ӽ��ͷǼ��Թ��ۼ������Դ��ǣ�
�����������Ӽ��ͷǼ��Թ��ۼ������Դ��ǣ� ![]() �����Ӽ������ۼ�����4��Ԫ�����ڱ��Т�A��λ�ڵ�2�С���A��λ�ڵ�13�У���Ԫ�����ڱ���ͼ��֪��X����Ϊ��A�壬��W��ദ��18�У�YԪ�ؿ���λ�ڵ�15��16��17���У����Դ��ǣ�15��16��17��
�����Ӽ������ۼ�����4��Ԫ�����ڱ��Т�A��λ�ڵ�2�С���A��λ�ڵ�13�У���Ԫ�����ڱ���ͼ��֪��X����Ϊ��A�壬��W��ദ��18�У�YԪ�ؿ���λ�ڵ�15��16��17���У����Դ��ǣ�15��16��17��

����Ŀ��CoCl2�� 6H2O��һ������Ӫ��ǿ������һ������ˮ�ܿ���Ҫ�ɷ�ΪCo2O3�� Co(OH)3,��������Fe2O3��Al2O3��MnO�ȣ���ȡCoCl2�� 6H2O�Ĺ����������£�
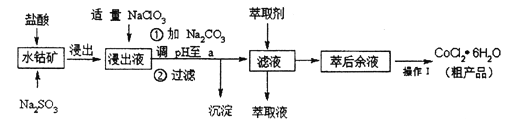
��֪���ٽ���Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Al3+����
�ڲ���������������������ʽ����ʱ��Һ��pH���±�(��������Ũ��Ϊ0.01 mol/L):
������ | Fe(OH)3 | Fe(OH)2 | Co (OH) 2 | Al(OH)3 | Mn(OH)2 |
��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��CoCl2�� 6H2O�۵�Ϊ86��,������110��120��ʱ��ʧȥ�ᾧˮ������ˮ�Ȼ��ܡ�
(1)д��������������Ҫ���������ӷ�Ӧ����ʽ��______________��
(2)��������������Һ���мӹ���NaC1O3ʱ�����ܻ����ɵ��к�������_______(�ѧʽ)��
(3)��ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ��������Һ���м�����ȡ����Ŀ����_______����ʹ�õ����pH��Χ�� ________(ѡ��������ĸ����
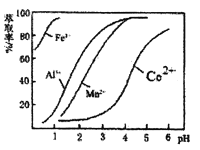
A. 2.0��2.5 B. 3.0��3.5 C. 4.0��4.5 D. 5.0��5.5
(4) ������1����________���Ƶõ�CoCl2�� 6H2O���ѹ��ɵ�ԭ����__________��
(5)Ϊ�ⶨ�ֲ�Ʒ��CoCl2�� 6H2O�ĺ�������ȡһ�������Ĵֲ�Ʒ����ˮ����������AgNO3��Һ�����ˡ�ϴ�ӣ���������ɺ����������ͨ�����㷢�ֲִ�Ʒ��CoCl2�� 6H2O��������������100%,��ԭ�������___________________��(��һ�����ɣ�