题目内容
已知HF的酸性比HCN的酸性强,现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,其pH值比较正确的是( )
| A、NaF<NaCN |
| B、NaF>NaCN |
| C、NaF=NaCN |
| D、无法比较 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:HF和HCN都是弱酸,HF的酸性比HCN的酸性强,物质的量浓度和体积均相同的NaF和NaCN两种溶液中阴离子水解程度F-<CN-;
解答:
解:HF和HCN都是弱酸,HF的酸性比HCN的酸性强,弱酸越弱对应酸根阴离子水解程度越大,所以物质的量浓度和体积均相同的NaF和NaCN两种溶液中阴离子水解程度F-<CN-,水解溶液呈碱性,NaCN溶液PH大于NaF溶液PH;
故选A.
故选A.
点评:本题考查了盐类水解原理分析判断,同浓度盐溶液,酸根离子水解程度取决于弱酸的强弱,掌握基础是关键,题目较简单.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、在反应KIO3+6 HI=KI+3I2十3 H2O中,每生成3mo1 I2转移的电子数为5NA |
| B、100mL 18.4mo1?L-1硫酸与足量Cu反应,生成SO2的分子数为0.92NA |
| C、1 L 0.1 moI?L-1的CH3COOH溶液中所含的离子和分子总数为0.1NA |
| D、将0.lmol FeC13滴人沸水中可制得0.1NA Fe(OH)3胶粒 |
下列说法正确的是(??)
| A、不含其他杂质的天然油脂属于纯净物 |
| B、肥皂的有效成分硬脂酸钠和甘油 |
| C、油脂的烃基部分饱和程度越大,熔点越低 |
| D、各种油脂水解后的产物中都有甘油 |
下列说法合理的是( )
| A、容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| B、用碱式滴定管量取12.85mL高锰酸钾溶液 |
| C、用湿润的PH试纸测定某NaOH溶液的PH |
| D、过滤时可用玻璃棒搅拌加快过滤速度 |
电泳实验发现,硫化砷胶粒向阳极移动,下列措施不能使硫化砷胶体凝聚的是( )
| A、加入Al2(SO4)3溶液 |
| B、加入硅酸胶体 |
| C、加热 |
| D、加入Fe(OH)3胶体 |
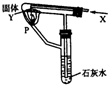 按如图的装置持续通入X气体并在支管P处点燃,实验时澄清石灰水变浑浊,则X、Y可能是( )
按如图的装置持续通入X气体并在支管P处点燃,实验时澄清石灰水变浑浊,则X、Y可能是( )| A、氢气和碳酸钠 |
| B、一氧化碳和碳酸钠 |
| C、一氧化碳和氧化铜 |
| D、氢气和氧化铁 |
下列有机物的命名中,不正确的是( )
| A、3,3-二甲基丁烷 |
| B、3-甲基-3-乙基戊烷 |
| C、4-甲基-3-乙基-2-己烯 |
| D、1-甲基-2-乙基-3-丙基苯 |
设阿伏加德罗常数为NA,下列说法中不正确的是( )
| A、15.6g Na2O2中含阴、阳离子数为0.6NA |
| B、标准状况下,11.2L CO2和O2的混合气体中含氧原子数为NA |
| C、8.7g MnO2和足量的浓盐酸反应,被氧化的Cl-为0.2NA |
| D、分子数为NA的CO、C2H4混合气体体积22.4L,其质量为28g |
下列说法错误的是( )
| A、SO2通入BaCl2溶液中无沉淀产生,通入FeCl3和BaCl2的混合溶液中有白色沉淀生成 |
| B、红磷在氯气中燃烧产生白色烟雾 |
| C、氯化碘(ICl)的化学性质与氯气相似,它跟水反应可生成HI和HClO |
| D、可在NaOH溶液液面上用倒扣漏斗装置吸收残余氯气 |