题目内容
对某未知有机物进行研究:称取该样品0.352 g,通入足量氧气流充分燃烧,将生成物先后通过无水硫酸铜和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收。下列说法错误的是
A.未知物中碳的质量分数是 41% B.未知物中含有C、H、O元素
C.未知物的实验式为C3H4O3 D.已有条件可确定未知物的分子式为C6H8O6
A.未知物中碳的质量分数是 41% B.未知物中含有C、H、O元素
C.未知物的实验式为C3H4O3 D.已有条件可确定未知物的分子式为C6H8O6
D
试题分析:无水硫酸铜吸水,即生成物水的质量是0.144g,物质的量是0.008mol。碱石灰吸收CO2,即二氧化碳的质量是0.528g,物质的量是0.012mol,则A、根据碳原子守恒可知未知物中碳的质量分数是
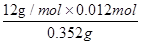 ×100%=41%,A正确;B、有机物中碳氢元素质量之和为0.016g+0.012mol×12g/mol=0.16g<0.352g,因此含有氧元素,B正确;C、其中氧原子的质量是0.352g-0.16g=0.192g,物质的量是0.012mol,因此碳氢氧原子的个数之比是0.012:0.016:0.012=3:4:3,即实验式为C3H4O3,C正确;D、无法确定有机物的相对分子质量,因此不能确定有机物的分子式,D不正确,答案选D。
×100%=41%,A正确;B、有机物中碳氢元素质量之和为0.016g+0.012mol×12g/mol=0.16g<0.352g,因此含有氧元素,B正确;C、其中氧原子的质量是0.352g-0.16g=0.192g,物质的量是0.012mol,因此碳氢氧原子的个数之比是0.012:0.016:0.012=3:4:3,即实验式为C3H4O3,C正确;D、无法确定有机物的相对分子质量,因此不能确定有机物的分子式,D不正确,答案选D。
练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目



 E.
E. F.
F.

 ,请写出它与NaOH溶液反应的化学方程式___________:
,请写出它与NaOH溶液反应的化学方程式___________: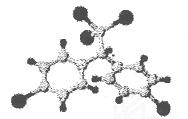
 是日常生活中常用的两种合成高分子材料,可由某烃经下列反应得到
是日常生活中常用的两种合成高分子材料,可由某烃经下列反应得到

 ,起始原料的某烃的结构简式
,起始原料的某烃的结构简式
 ;
; 
