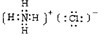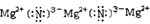题目内容
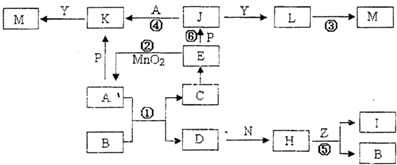
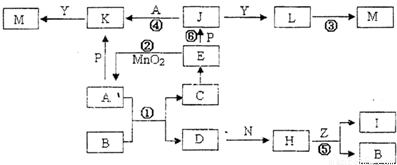
下图中,A、D为气体非金属单质,N、P是金属单质;M为红褐色沉淀;B、E为有刺激性气味的气体;通常状况下,Z为液体;C是由三咱短周期非金属元素组成的离子化合物;I、L为白色沉淀.反应②、⑥均可用于实验室制取某种常见气体;工业上以D为原料生产B(图中部分反应物和生成物没有列出).

请按要求回答:
(1)写出D的结构式______,C的电子式______;H的电子式______.
(2)上述①--⑥反应中属于氧化还原反应的有______(填写序号),其中反应______可
用于除去K溶液中含有的少量J(填写序号).
(3)反应②的离子方程式为了______.
实验室制B的化学方程式为______.
(4)生活中K可用作净水剂,用离子方程式表示其原理______.
(5)写出A、M和氢氧化钾在一定条件下反应生成K2PO4(P为题中P物质的元素符号,答题时用所对应的元素符号表示)______.
接:根据题意M为红褐色沉淀即为氢氧化铁,B、E为有刺激性气味的气体,即为氨气或氯化氢或是二氧化硫等,②、⑥均可用于实验室制取某种常见气体,所以推得E为HCl,A为Cl2,则P一定是金属铁,所以J是氯化亚铁,Y是一种强碱,C是由三中短周期非金属元素组成的离子化合物,所以是氯化铵,所以B是氨气,D是氮气,工业上以氮气为原料生产氨气,Z为液体,应该是水,所以金属N是金属镁,H是氮化镁,I是氢氧化镁.
(1)氮气中含有叁键,结构式为N≡N,氯化铵是含有离子键和共价键的离子化合物,电子式为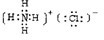 ,
,
氮化镁属于离子化合物,含有离子键,电子式为: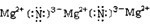 ,故答案为:N≡N;
,故答案为:N≡N;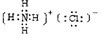 ;
;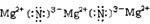 ;
;
(2)有化合价变化的反应是氧化还原反应,反应①②③④⑥中的氯元素、氯元素(锰元素)、铁元素(氧元素)、铁元素、铁元素(氯元素)化合价均有变化,属于氧化还原反应,除去三氯化铁中的氯化亚铁可以向其中滴加氯水来实现,故答案为:①②③④⑥;④;
(3)实验室制氯气的原理方程式为:4H++MnO2 Cl2↑+Mn2++2H2O,实验室制取氨气的化学方程式为:Ca(OH)2+2NH4Cl
Cl2↑+Mn2++2H2O,实验室制取氨气的化学方程式为:Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O,故答案为:4H++MnO2
CaCl2+2NH3↑+2H2O,故答案为:4H++MnO2 Cl2↑+Mn2++2H2O;Ca(OH)2+2NH4Cl
Cl2↑+Mn2++2H2O;Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(4)氯化铁中的铁离子能水解生成具有净水作用的氢氧化铁胶体,实质是:Fe3++3H2O Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O
Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O Fe(OH)3(胶体)+3H+;
Fe(OH)3(胶体)+3H+;
(5)氯气、氢氧化铁、和氢氧化钾在一定条件下反应生成K2PO4的方程式为:3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl,故答案为:3Cl2+2Fe(OH)3+10KOH
2K2FeO4+6KCl,故答案为:3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl.
2K2FeO4+6KCl.
分析:推断题要注意寻找解题的突破口,注意框图中隐藏的已知条件,如本题中红褐色沉淀是氢氧化铁,反应②、⑥均可用于实验室制取某种常见气体,可推知E为HCl,P是Fe,根据物质之间的性质结合物质之间的转化来获得其他物质的化学式.
点评:本题是一道框图推断题,综合性较强,考查学生分析和解决问题的能力以及知识的归纳能力,难度大.
(1)氮气中含有叁键,结构式为N≡N,氯化铵是含有离子键和共价键的离子化合物,电子式为
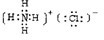 ,
,氮化镁属于离子化合物,含有离子键,电子式为:
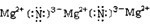 ,故答案为:N≡N;
,故答案为:N≡N;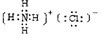 ;
;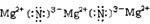 ;
;(2)有化合价变化的反应是氧化还原反应,反应①②③④⑥中的氯元素、氯元素(锰元素)、铁元素(氧元素)、铁元素、铁元素(氯元素)化合价均有变化,属于氧化还原反应,除去三氯化铁中的氯化亚铁可以向其中滴加氯水来实现,故答案为:①②③④⑥;④;
(3)实验室制氯气的原理方程式为:4H++MnO2
 Cl2↑+Mn2++2H2O,实验室制取氨气的化学方程式为:Ca(OH)2+2NH4Cl
Cl2↑+Mn2++2H2O,实验室制取氨气的化学方程式为:Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O,故答案为:4H++MnO2
CaCl2+2NH3↑+2H2O,故答案为:4H++MnO2 Cl2↑+Mn2++2H2O;Ca(OH)2+2NH4Cl
Cl2↑+Mn2++2H2O;Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;(4)氯化铁中的铁离子能水解生成具有净水作用的氢氧化铁胶体,实质是:Fe3++3H2O
 Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O
Fe(OH)3(胶体)+3H+,故答案为:Fe3++3H2O Fe(OH)3(胶体)+3H+;
Fe(OH)3(胶体)+3H+;(5)氯气、氢氧化铁、和氢氧化钾在一定条件下反应生成K2PO4的方程式为:3Cl2+2Fe(OH)3+10KOH
 2K2FeO4+6KCl,故答案为:3Cl2+2Fe(OH)3+10KOH
2K2FeO4+6KCl,故答案为:3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl.
2K2FeO4+6KCl.分析:推断题要注意寻找解题的突破口,注意框图中隐藏的已知条件,如本题中红褐色沉淀是氢氧化铁,反应②、⑥均可用于实验室制取某种常见气体,可推知E为HCl,P是Fe,根据物质之间的性质结合物质之间的转化来获得其他物质的化学式.
点评:本题是一道框图推断题,综合性较强,考查学生分析和解决问题的能力以及知识的归纳能力,难度大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
(15分,每小题各3分)下图中,A到L为常见物质或该物质的水溶液,B在A气体
中燃烧产生棕黄色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,组成J的
元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色。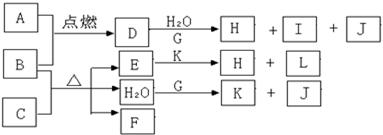
|
(1)J的结构式为 。
(2)K的电子式为 ,属于 晶体,所含的化学键有 。
(3)若D的水溶液呈黄色,沉淀H的化学式为 。
(4)若D的水溶液呈蓝色,B与C反应的化学方程式为 。
(5)G与H2O反应的离子方程式为 。