题目内容
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题。
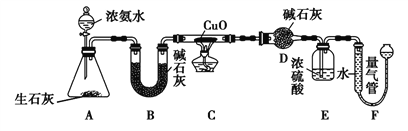
(1)写出A装置中发生反应的化学方程式__________。
(2)实验中观察到C装置中黑色CuO粉末变为红色固体,量气管中有无色无味的气体产生,上述现象证明NH3具有____性,写出相应的化学方程式______。
(3)读取气体体积前,对F装置进行的操作是慢慢上下移动右边的漏斗,使左右两管液面相平,其目的是________________。
(4)E装置的作用是___________;量气管中有空气,对实验______(填“有”或“无”)影响。
(5)实验完毕,若测得干燥管D增重mg,F装置测得气体的体积为VL(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、V的代数式表示)。若拆掉B装置,测得的结果____(填“偏大”“偏小”或“无影响”)。
【答案】 NH3·H2O(浓)+CaO![]() Ca(OH)2+NH3↑ 还原 3CuO+2NH3
Ca(OH)2+NH3↑ 还原 3CuO+2NH3![]() 3Cu+N2+3H2O 使收集N2的压强与外界大气压相等 吸收NH3、防止F中水蒸气进入D 无 9V︰11.2m 偏小
3Cu+N2+3H2O 使收集N2的压强与外界大气压相等 吸收NH3、防止F中水蒸气进入D 无 9V︰11.2m 偏小
【解析】(1).将浓氨水滴入锥形瓶中,生石灰与水反应生成氢氧化钙并放出大量的热,使NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-平衡逆向移动,生成氨气,总反应方程式为:NH3·H2O(浓)+CaO
NH4++OH-平衡逆向移动,生成氨气,总反应方程式为:NH3·H2O(浓)+CaO![]() Ca(OH)2+NH3↑,故答案为:NH3·H2O(浓)+CaO
Ca(OH)2+NH3↑,故答案为:NH3·H2O(浓)+CaO![]() Ca(OH)2+NH3↑;
Ca(OH)2+NH3↑;
(2).实验中观察到C装置中黑色CuO粉末变为红色固体,说明有Cu生成,量气管中有无色无味的气体产生,说明生成了N2,则氨气中的氮元素化合价从-3价升高到0价,氨气体现了还原性,该反应的化学方程式为:3CuO+2NH3![]() 3Cu+N2+3H2O,故答案为:还原;3CuO+2NH3
3Cu+N2+3H2O,故答案为:还原;3CuO+2NH3![]() 3Cu+N2+3H2O;
3Cu+N2+3H2O;
(3).读取气体体积前,对F装置进行的操作是慢慢上下移动右边的漏斗,使左右两管液面相平,其目的是使量气管内与外界大气压相等,保持压强平衡,故答案为:使收集N2的压强与外界大气压相等;
(4).根据流程可知,浓硫酸的作用是吸收过量的氨气并阻止F中的水蒸气进入D中,因利用的是排水法测量N2的体积,则量气管中有空气,对实验无影响,故答案为:吸收NH3、防止F中水蒸气进入D;无;
(5). 干燥管D中盛装碱石灰,吸收混合气体中的水蒸气,若测得干燥管D增重mg,则水的物质的量=![]() ,装置F测得的气体为N2,体积为VL(已折算成标准状况),则N2物质的量=
,装置F测得的气体为N2,体积为VL(已折算成标准状况),则N2物质的量=![]() ,依据元素守恒得到氮原子和氢原子物质的量之比为(
,依据元素守恒得到氮原子和氢原子物质的量之比为(![]() ×2):(
×2):( ![]() ×2)=
×2)= ![]() ;B装置的作用是防止A中水蒸气进入后续装置中影响实验效果,若拆掉B装置,则测得的水偏多,结果偏小,故答案为:9V︰11.2m;偏小。
;B装置的作用是防止A中水蒸气进入后续装置中影响实验效果,若拆掉B装置,则测得的水偏多,结果偏小,故答案为:9V︰11.2m;偏小。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某合金与铁的物理性质的比较如下表所示,还知该合金耐腐蚀、强度大,从以上性能看,该合金不适合做
熔点/℃ | 密度(g/cm3) | 硬度(金刚石为10) | 导电性(银为100) | |
某合金 | 2500 | 3.00 | 7.4 | 2.3 |
铁 | 1535 | 7.86 | 4.5 | 17 |
A. 导线 B. 门窗框 C. 炉具 D. 飞机外壳