题目内容
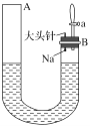
【题目】如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。回答下列问题:
(1)钠与水反应的化学方程式为_____________。
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是_________。
②能证明钠的熔点低的现象是_________。
③能证明有氢氧化钠生成的现象是__________。
④能证明有气体产生的现象是A端液面________(填“上升”“下降”或“不变”,下同),B端液面________。
【答案】2Na+2H2O=2NaOH+H2↑ 钠浮在水面上 钠熔化为光亮的小球 溶液呈红色 上升 下降
【解析】
本题主要考察金属钠和水的反应,该反应的现象为“浮”、“响”、“游”、“熔”、“红”。“浮”指钠块浮在水面上;“响”是因为反应放热,且不断有H2生成;“游”是产生的H2不断推动钠块来回移动;“熔”是因为钠块的熔点很低,反应放热使钠块熔化;“红”是因为反应生成了NaOH,使事先加入的酚酞变红。
(1)钠与水反应生成NaOH和H2,其化学方程式为:2Na+2H2O=2NaOH+H2↑;
(2)①钠浮在水面上,证明钠的密度比水小;
②钠熔化为光亮的小球,证明钠的熔点低;
③反应后溶液呈红色,证明有氢氧化钠生成;
④B端压强增大,液面下降,A端液面上升,证明有气体生成。

【题目】下列“解释或结论”与“实验操作及现象”不相符的一组是
序号 | 实验操作及现象 | 解释或结论 |
A | 浓硫酸滴到纸张上,纸变黑 | 浓硫酸有脱水性 |
B | 向紫色石蕊溶液中加入氯水,溶液先变红,随后褪色 | 氯水中含有酸性物质和 漂白性物质 |
C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的气体 | 该溶液中一定有CO32- |
D | 向某溶液中加入浓NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中一定含有NH |
A.AB.BC.CD.D