题目内容
2010年亚运会在我国广州成功举办,整个亚运会体现了环保理念.(1)广州亚运会火炬“潮流”采用了丙烷(C3H8)作为燃料,燃烧后的产物为水和二氧化碳.在298K时,1mol丙烷完全燃烧生成CO2和液态水放出2221.5kJ的热量,则该反应的热化学方程式为______.
又知:在298K时C3H8(g)=C3H6(g)+H2(g)△H=124.2kJ?mol-1,H2(g)+
 O2(g)=H2O(I)△H=-285.8kJ?mol-1,则l mo1C3H6完全燃烧生成CO2和液态水时放出的热量是______kJ.
O2(g)=H2O(I)△H=-285.8kJ?mol-1,则l mo1C3H6完全燃烧生成CO2和液态水时放出的热量是______kJ.(2)广州是一座美丽的海滨城市,海水资源非常丰富.
①海洋电池是以铝为负极,铂网为正极,海水为电解质溶液,空气中氧气与铝反应产生电流,电池总反应为4Al+3O2+6H2O=4Al(OH)3,下列说法正确的是______(填写序号字母);
a.电池工作时,电流由铝电极沿导线流向铂电极
b.铂电极采用网状比块状更利于O2放电
c.海水中的OH-向铝电极方向移动
②用惰性电极电解200mL l.5mol/L食盐水;电解2min时,两极共收集到448mL气体(标准状况下).写出该电解反应的离子方程式______ 2OH-+H2↑+Cl2↑
【答案】分析:(1)根据热化学方程式的含义以及书写方法来回答;
(2)①a.原电池工作时,电流由负极沿导线流向正极;
b.铂电极采用网状能增大气体的面积;
c.原电池工作时,电解质中的阴离子移向负极.
②根据电解食盐水的总反应来及计算回答.
解答:解:(1)在298K时,1mol丙烷完全燃烧生成CO2和液态水放出2221.5kJ的热量,则该反应的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1;
(2)①铝为负极,铂网为正极,海水为电解质溶液形成的原电池中,
a.原电池工作时,电流由负极沿导线流向正极,即电流由铂电极沿导线流向铝电极,故a错误;
b.铂电极采用网状能增大气体的面积,网状比块状更利于O2放电,故b正确;
c.原电池工作时,电解质中的阴离子移向负极,所以海水中的OH-向铝电极方向移动,故c正确;
故答案为:bc;
②电解氯化钠溶液反应的离子方程式为:2Cl-+2H2O 2OH-+H2↑+Cl2↑,根据总反应当两极上共收集到0.448L即0.02 mol气体时,则生成的氯气和氢气均是0.01mol,所以生成氢氧化钠的物质的量是0.02mol,所以氢氧化钠的浓度C=
2OH-+H2↑+Cl2↑,根据总反应当两极上共收集到0.448L即0.02 mol气体时,则生成的氯气和氢气均是0.01mol,所以生成氢氧化钠的物质的量是0.02mol,所以氢氧化钠的浓度C=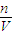 =
= =0.1mol/L,所以pH=13,故答案为:2Cl-+2H2O
=0.1mol/L,所以pH=13,故答案为:2Cl-+2H2O 2OH-+H2↑+Cl2↑;13.
2OH-+H2↑+Cl2↑;13.
点评:本题是对热化学和电化学知识的综合考查,要求学生具有分析和解决问题的能力,难度不是很大.
(2)①a.原电池工作时,电流由负极沿导线流向正极;
b.铂电极采用网状能增大气体的面积;
c.原电池工作时,电解质中的阴离子移向负极.
②根据电解食盐水的总反应来及计算回答.
解答:解:(1)在298K时,1mol丙烷完全燃烧生成CO2和液态水放出2221.5kJ的热量,则该反应的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1,
故答案为:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l),△H=-2221.5kJ?mol-1;
(2)①铝为负极,铂网为正极,海水为电解质溶液形成的原电池中,
a.原电池工作时,电流由负极沿导线流向正极,即电流由铂电极沿导线流向铝电极,故a错误;
b.铂电极采用网状能增大气体的面积,网状比块状更利于O2放电,故b正确;
c.原电池工作时,电解质中的阴离子移向负极,所以海水中的OH-向铝电极方向移动,故c正确;
故答案为:bc;
②电解氯化钠溶液反应的离子方程式为:2Cl-+2H2O
 2OH-+H2↑+Cl2↑,根据总反应当两极上共收集到0.448L即0.02 mol气体时,则生成的氯气和氢气均是0.01mol,所以生成氢氧化钠的物质的量是0.02mol,所以氢氧化钠的浓度C=
2OH-+H2↑+Cl2↑,根据总反应当两极上共收集到0.448L即0.02 mol气体时,则生成的氯气和氢气均是0.01mol,所以生成氢氧化钠的物质的量是0.02mol,所以氢氧化钠的浓度C=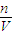 =
= =0.1mol/L,所以pH=13,故答案为:2Cl-+2H2O
=0.1mol/L,所以pH=13,故答案为:2Cl-+2H2O 2OH-+H2↑+Cl2↑;13.
2OH-+H2↑+Cl2↑;13.点评:本题是对热化学和电化学知识的综合考查,要求学生具有分析和解决问题的能力,难度不是很大.

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目