题目内容
磷单质及其化合物有广泛应用.白磷(P4)是磷的单质之一,易氧化,与Cl2单质反应通常生成PCl3或PCl5.
(1)6.20 g白磷在足量氧气中完全燃烧生成氧化物,反应所消耗的氧气在标准状况下的体积为________L.上述燃烧产物溶于水配成100.0 mL磷酸(H3PO4)溶液,需要的玻璃仪器除烧杯,玻璃棒外,还需要________,该磷酸溶液的物质的量浓度为________.
(2)含0.300 mol H3PO4的水溶液滴加到含0.500 mol Ca(OH)2的悬浮液中,反应恰好完全,生成l种难溶盐和16.2 g H2O.该难溶盐的化学式可表示为________.
(3)同磷灰石[主要成分Ca5(PO4)3F(s)]在高温下制备P4的化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)![]() 3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)上述反应中,副产物矿渣可用来________.
3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)上述反应中,副产物矿渣可用来________.
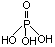
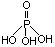
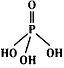
(4)三聚磷酸可视为三个磷酸分子(磷酸结构式见下图)之间脱去两个水分子产物,其结构式为________.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为________
.
(5)次磷酸钠(NaH2PO2)可用于化学镀镍.
化学镀镍的溶液中含有
Ni2+和H2PO2-,在酸性条件下发生下述反应,请配平该离子方程式.________Ni2++________H2PO2-+________→________Ni++________H2PO3-+________
解析:
|
(1)5.6(1分);100.0 mL容量瓶(1分);胶头滴管(1分);2.00 mol·L-1(1分); (2)Ca5(PO4)3(OH);(1分) (3)水泥(1分); (4) (5)2Ni2++1H2PO2-+1H2O→2Ni++1H2PO3-+2H+(2分) |

 (1分);Na5P3O10;(1分)
(1分);Na5P3O10;(1分)