题目内容
某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质。设计了如下图所示装置进行实验.
已知:1.0 mol/L的Fe(NO3)3溶液的pH=1。
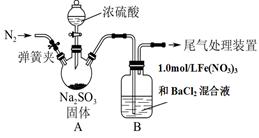
请回答:
(1)装置A中用于添加浓硫酸的仪器名称为 。
(2)实验前鼓入N2的目的是 。
(3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性。
(4)分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与NO3-反应;
①若观点1正确,除产生沉淀外,还应观察到的现象是 。
②按观点2,装置B中反应的离子方程式是 ,
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是(填序号) 。
已知:1.0 mol/L的Fe(NO3)3溶液的pH=1。

请回答:
(1)装置A中用于添加浓硫酸的仪器名称为 。
(2)实验前鼓入N2的目的是 。
(3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性。
(4)分析B中产生白色沉淀的原因。
观点1:SO2与Fe3+反应;
观点2:在酸性条件下SO2与NO3-反应;
①若观点1正确,除产生沉淀外,还应观察到的现象是 。
②按观点2,装置B中反应的离子方程式是 ,
③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是(填序号) 。
| A.1 mol/L稀硝酸 |
| B.1.5 mol/L Fe(NO3)2溶液 |
| C.6.0 mol/L NaNO3溶液和0.2 mol/L盐酸等体积混合的溶液 |
| D.3.0 mol/L NaNO3溶液和0.1mol/L硫酸等体积混合的溶液 |
(1)分液漏斗(2分)
(2)排净装置中的空气,防止溶液中SO2被空气中的O2氧化而干扰实验(2分)
(3)BaSO4(1分);还原(1分)
(4)①静置一段时间后,溶液由棕黄色变为浅绿色(2分)
②3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+
或3SO2+2NO3-+2H2O=3SO42-+2NO+4H+;Ba2++SO42- = BaSO4↓(2分)
③ C(2分)
(2)排净装置中的空气,防止溶液中SO2被空气中的O2氧化而干扰实验(2分)
(3)BaSO4(1分);还原(1分)
(4)①静置一段时间后,溶液由棕黄色变为浅绿色(2分)
②3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO+4H+
或3SO2+2NO3-+2H2O=3SO42-+2NO+4H+;Ba2++SO42- = BaSO4↓(2分)
③ C(2分)
试题分析:(2)反应前要充入N2,排除装置A中的空气,反应对实验的干扰。
(3)硝酸具有氧化性,白色沉淀为BaSO4,说明SO2具有还原性。
(4)经过分析,各个观点,得出观点1是SO2和Fe3+、酸性条件下NO3-都反应。
①Fe3+把SO2氧化,离子方程式是SO2+2Fe3++Ba2++2H2O=BaSO4↓+2Fe2++4H+。
②Fe(NO3)3中有Fe3+,a错;NO3-在酸性条件下有氧化性,b错。故选c。
SO2制备 Fe3+、NO3-的氧化性。2制备 Fe3+、NO3-的氧化性。

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目

 Na2O2
Na2O2 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑

 CO2 + H2
CO2 + H2
 MnCl2 +Cl2↑+2H2 O,氧化剂和还原剂的物质的量比为
MnCl2 +Cl2↑+2H2 O,氧化剂和还原剂的物质的量比为