题目内容
下列操作能达到实验目的的是
| A.称取1.06g碳酸钠固体溶于100mL水中,配制成0.1mol/ L的溶液 |
| B.向一定量的NaOH溶液中通入足量的CO2以制取纯净的Na2CO3溶液 |
| C.向某无色溶液中加入硝酸酸化的BaCl2溶液,以检验溶液中是否含有SO42-离子 |
| D.向水中加入乙醇来减缓钠与水的反应速度 |
D
A不正确,溶液的体积是0.1L,而不是溶剂是0.1L;B不正确,CO2过量时,生成的碳酸氢钠;C不正确,一方面不能排除Ag+,另一方面硝酸具有氧化性,能氧化SO32-,所以也不能排除SO32-,所以正确的答案选D。

练习册系列答案
相关题目
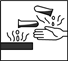



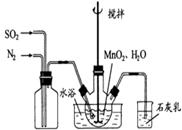
 换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。
换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 。