题目内容
【题目】“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体,CO2的综合利用是解决温室及能源问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:
CH3OH(g)+![]() O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1
O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1
H2(g)+![]() O2(g) = H2O(1) △H2=bkJmol-1
O2(g) = H2O(1) △H2=bkJmol-1
H2O(g) = H2O(l) △H3=ckJmol-1
则 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=__________kJmol-1
CH3OH(g)+H2O(g) △H=__________kJmol-1
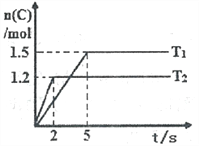
(2)CO2催化加氢也能合成低碳烯烃: 2CO2(g)+6H2(g)![]() C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。
C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。

(3)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应 A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+ H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图2所示。

① 由图2可知温度升高CO的产率上升,其主要原因可能是__________________。
② 由图2可知获取CH3OH最适宜的温度是________________,下列措施有利于提高CO2转化为CH3OH的平衡转化率的措施有__________________。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
(4)在催化剂表面通过施加电压可将溶解在水中的二氧化碳直接转化为乙醇,则生成乙醇的电极反应式为______________________________________________________。
(5)由CO2制取C的太阳能工艺如图3所示。“热分解系统”发生的反应为:2Fe3O4![]() 6FeO+O2↑,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
6FeO+O2↑,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。

【答案】 3b-a-c H2O 反应B正反应是吸热反应,温度升高平衡正向移动,CO产率升高 250℃ BD 2CO2 + 12H++12e-=C2H5OH+3H2O 2 mol 6FeO+CO2![]() 2Fe3O4+C
2Fe3O4+C
【解析】(1)已知:①CH3OH(g)+![]() O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1,②H2(g)+
O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1,②H2(g)+![]() O2(g) = H2O(1) △H2=bkJmol-1,③H2O(g) = H2O(l) △H3=ckJmol-1,根据盖斯定律,由②×3-①-③可得 CO2(g)+3H2(g)
O2(g) = H2O(1) △H2=bkJmol-1,③H2O(g) = H2O(l) △H3=ckJmol-1,根据盖斯定律,由②×3-①-③可得 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ,则△H=(bkJmol-1)×3-(akJmol-1)-(ckJmol-1)=(3b-a-c)kJmol-1;
CH3OH(g)+H2O(g) ,则△H=(bkJmol-1)×3-(akJmol-1)-(ckJmol-1)=(3b-a-c)kJmol-1;
(2)随着温度升高,氢气的物质的量逐渐增多,因氢气为反应物,则另一条逐渐增多的曲线为CO2,由计量数关系可知b为水,c为C2H4的变化曲线;
(3)①由图2可知 反应B正反应是吸热反应,温度升高平衡正向移动,CO产率升高;
② 由图2可知获取CH3OH产率最高对应的温度是250℃,则选择最适宜的温度是250℃;A.使用催化剂,平衡不移动,不能提高转化率,故A错误;B.增大体系压强,平衡正向移动,可增大转化率,故B正确;C.增大 CO2和H2的初始投料比,可增大氢气的转化率,二氧化碳的转化率减小,故C错误;D.投料比不变,增加反应物的浓度,衡正向移动,可增大转化率,故D正确;故答案为BD;
(4)二氧化碳直接转化为乙醇,是还原过程,发生在电解池的正极,其电极反应式为 2CO2+12H++12e-=C2H5OH+3H2O;
(5)反应2Fe3O4![]() 6FeO+O2↑中O元素化合价由-2价升高到0价,由方程式可知,2molFe3O4参加反应,生成1mol氧气,转移4mol电子,则每分解lmolFe3O4转移电子的物质的量为2mol;由示意图可知,重整系统中CO2和FeO反应生成Fe3O4和C,反应的方程式为6FeO+CO2
6FeO+O2↑中O元素化合价由-2价升高到0价,由方程式可知,2molFe3O4参加反应,生成1mol氧气,转移4mol电子,则每分解lmolFe3O4转移电子的物质的量为2mol;由示意图可知,重整系统中CO2和FeO反应生成Fe3O4和C,反应的方程式为6FeO+CO2![]() 2Fe3O4+C。
2Fe3O4+C。

【题目】现有部分短周期元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第3周期元素的简单离子中半径最小 |
W | 质量数为31,原子核内中子数比质子数多1 |
(1)写出元素T的原子结构示意图:__________________________。
(2)元素Y与元素Z相比,金属性较强的是________________(用元素符号表示),下列表述中能证明这一事实的是________________(填字母)。
a.Y的化合价比Z低
b.Y单质与水反应比Z单质剧烈
c.Y的最高价氧化物对应水化物的碱性比Z的强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,则该该化合物的化学式为:_________________。
(4)T与W形成的化合物被潮解后的产物是________________(填化学式)。
(5)元素T与氢元素以原子个数1:1化合形成化合物Q,元素X与氢元素以原子个数1∶2化合形成常用于火箭燃料的化合物W,Q与W发生氧化还原反应,生成X的单质和T的另一种氢化物,写出该反应的化学方程式:______________________________________。
【题目】气体打火机使用的燃料要求在室温下为气态,稍一加压,就变成液体,一减压(打开阀门)就汽化并易燃烧。下表中的有机物能较好地满足这些要求的是( )
选项 | A | B | C | D |
分子式 | C2H6 | C3H8 | C4H10 | C5H12 |
熔点/℃ | -183.3 | -181.7 | -138.4 | -127.9 |
沸点/℃ | -88.6 | -42.1 | -0.5 | 36.1 |
A. A B. B C. C D. D