题目内容
对于反应2N(g)+3M(g)?XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后达平衡时生成2.4mol气体R,并测得Q的浓度为0.4mol/L,则X的值为
2
2
,M的转化率为80%
80%
,用M物质表示的反应速率vM=0.3mol/(L.min)
0.3mol/(L.min)
.分析:容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后达平衡时生成2.4mol气体R,测得Q的浓度为0.4mol/L,Q为0.4mol/L×4L=1.6mol,则
2N(g)+3M(g)?XQ(g)+3R(g),
开始 2 3 0 0
转化1.6 2.4 1.6 2.4
平衡0.4 0.6 1.6 2.4
以此计算.
2N(g)+3M(g)?XQ(g)+3R(g),
开始 2 3 0 0
转化1.6 2.4 1.6 2.4
平衡0.4 0.6 1.6 2.4
以此计算.
解答:解:容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后达平衡时生成2.4mol气体R,测得Q的浓度为0.4mol/L,Q为0.4mol/L×4L=1.6mol,则
2N(g)+3M(g)?XQ(g)+3R(g),
开始 2 3 0 0
转化1.6 2.4 1.6 2.4
平衡0.4 0.6 1.6 2.4
由转化的量可知,消耗N和生成Q相同,则化学计量数相同,即X=2,
M的转化率为
×100%=80%,
用M物质表示的反应速率vM=
=0.3mol/(L.min),
故答案为:2;80%;0.3mol/(L.min).
2N(g)+3M(g)?XQ(g)+3R(g),
开始 2 3 0 0
转化1.6 2.4 1.6 2.4
平衡0.4 0.6 1.6 2.4
由转化的量可知,消耗N和生成Q相同,则化学计量数相同,即X=2,
M的转化率为
| 2.4mol |
| 3mol |
用M物质表示的反应速率vM=
| ||
| 2min |
故答案为:2;80%;0.3mol/(L.min).
点评:本题考查化学平衡的计算,明确化学平衡三段法计算格式及转化率、反应速率的计算方法即可解答,注意格式规范,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
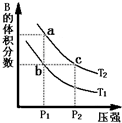 对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.
对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题. XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后达平衡时生成2.4 mol气体R,并测得Q的浓度为0.4mol/L,则X的值为
,M的转化率为 ,用M物质表示的反应速率vM=
XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后达平衡时生成2.4 mol气体R,并测得Q的浓度为0.4mol/L,则X的值为
,M的转化率为 ,用M物质表示的反应速率vM=
 XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后
XQ(g)+3R(g),在容积为4L的密闭容器中,将2mol气体N和3mol气体M混合,当反应经2min后 达平衡时生成2.4 mol气体R,并测得Q的浓度为0.4mol/L,则X的值为 ,M的转化率为 ,用M物质表示的反应速率vM=
达平衡时生成2.4 mol气体R,并测得Q的浓度为0.4mol/L,则X的值为 ,M的转化率为 ,用M物质表示的反应速率vM=