题目内容
(8分)A、B、C、D是常见不同主族的短周期元素,它们的原子序数逐渐增大,其中只有一种是金属元素。A是所有元素中原子半径最小的,C元素原子最外层电子数是D元素原子最外层电子数的一半,D元素最外层电子数是K层电子数的3倍,B元素原子的最外层电子数比D的少2个。E是与D同主族的短周期元素且原子半径小于D。请回答下列问题:
(1)五种元素中的三种组成的易溶于水的物质中,能促进水电离的物质M是 (写化学式,写一个即可,下同),能抑制水电离的物质N是 。25℃时,pH=a的M溶液中水电离出的H+浓度与pH=a的N溶液中水电离出的H+浓度之比为 。
(2)甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同。回答问题:
①向丙溶液中缓慢滴加过量的乙溶液过程中发生反应的离子方程式:
。
②向甲溶液中缓慢滴加等物质的量的丙溶液后,所得溶液中离子浓度由大到小的顺序为 。
(1)五种元素中的三种组成的易溶于水的物质中,能促进水电离的物质M是 (写化学式,写一个即可,下同),能抑制水电离的物质N是 。25℃时,pH=a的M溶液中水电离出的H+浓度与pH=a的N溶液中水电离出的H+浓度之比为 。
(2)甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,且丙用量不同,反应的产物不同。回答问题:
①向丙溶液中缓慢滴加过量的乙溶液过程中发生反应的离子方程式:
。
②向甲溶液中缓慢滴加等物质的量的丙溶液后,所得溶液中离子浓度由大到小的顺序为 。
(1)Al2(SO4)3 H2SO4或H2SO3或H2CO3(其它合理答案也可)1014—2a(每空1分)
(2)① 4H+ + AlO2- = Al3+ + 2H2O (1分)
Al3+ + 3 AlO2- +6H2O = 4Al(OH)3↓ (2分)
②c(Na+)>c(SO42-)>c(HCO3-)>c(OH-)>c(H+)>(CO32-) (2分)
(2)① 4H+ + AlO2- = Al3+ + 2H2O (1分)
Al3+ + 3 AlO2- +6H2O = 4Al(OH)3↓ (2分)
②c(Na+)>c(SO42-)>c(HCO3-)>c(OH-)>c(H+)>(CO32-) (2分)
由A是所有元素中原子半径最小的可以推出A为H元素;D元素最外层电子数是K层电子数的3倍,可以推出D为VIA族元素,E与D同主族且原子半径小于D,可以推出D为S元素,E为O元素; B元素原子的最外层电子数比D的少2个,C元素原子最外层电子数是D元素原子最外层电子数的一半,并且原子序数C大于B,可以推出B为C元素,C为Al元素。
问题(1)五种元素中的三种组成的易溶于水的物质中,能促进水电离的物质M应该属于能水解的盐类比如Al2(SO4)3;易溶于水且能抑制水电离的物质N应该属于酸类如H2SO4、H2SO3、H2CO3、CH3COOH等;25℃时,pH=a的M溶液中水电离出的H+浓度为10-amol/L,pH=a的N溶液中水电离出的H+浓度为10-14/10-a=10a-14mol/L,二者之比为1014—2a。
问题(2)由甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,则可以推知甲为Na2CO3、乙为NaAlO2、丙为NaHSO4。
①向NaHSO4溶液中缓慢滴加过量的NaAlO2溶液,由于开始时NaHSO4过量,所以先发生4H+ + AlO2- = Al3+ + 2H2O,当将NaHSO4反应完之后,再发生Al3+ + 3 AlO2- +6H2O = 4Al(OH)3↓。
②向Na2CO3溶液中缓慢滴加等物质的量的NaHSO4溶液后,溶液中存在的物质是NaHCO3和Na2SO4 。HCO3-水解使溶液显碱性,HCO3-电离产生H+和CO32-,加上水电离产生的H+,使得c(H+) >c(CO32-),所以溶液中离子浓度由大到小的顺序为c(Na+)>c(SO42-)>c(HCO3-)>c(OH-)>c(H+)> c(CO32-)。
问题(1)五种元素中的三种组成的易溶于水的物质中,能促进水电离的物质M应该属于能水解的盐类比如Al2(SO4)3;易溶于水且能抑制水电离的物质N应该属于酸类如H2SO4、H2SO3、H2CO3、CH3COOH等;25℃时,pH=a的M溶液中水电离出的H+浓度为10-amol/L,pH=a的N溶液中水电离出的H+浓度为10-14/10-a=10a-14mol/L,二者之比为1014—2a。
问题(2)由甲、乙、丙分别是B、C、D三种元素最高价含氧酸的钠盐,甲、乙都能与丙发生反应,则可以推知甲为Na2CO3、乙为NaAlO2、丙为NaHSO4。
①向NaHSO4溶液中缓慢滴加过量的NaAlO2溶液,由于开始时NaHSO4过量,所以先发生4H+ + AlO2- = Al3+ + 2H2O,当将NaHSO4反应完之后,再发生Al3+ + 3 AlO2- +6H2O = 4Al(OH)3↓。
②向Na2CO3溶液中缓慢滴加等物质的量的NaHSO4溶液后,溶液中存在的物质是NaHCO3和Na2SO4 。HCO3-水解使溶液显碱性,HCO3-电离产生H+和CO32-,加上水电离产生的H+,使得c(H+) >c(CO32-),所以溶液中离子浓度由大到小的顺序为c(Na+)>c(SO42-)>c(HCO3-)>c(OH-)>c(H+)> c(CO32-)。

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
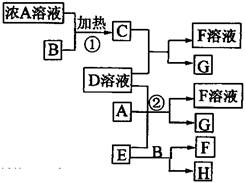
 请回答下列问题:
请回答下列问题: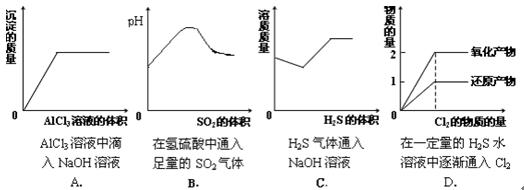
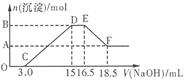
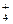 中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是
中的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中逐滴加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图,则下列说法中不正确的是