题目内容
下列叙述正确 的是
| A.由于Ksp(BaSO4)=" 1.1" ×10-10 小于Ksp(BaCO3)=" 5.1" ×10-9,则不能使BaSO4沉淀转化为BaCO3沉淀 |
| B.在中和热测定的实验中,将NaOH溶液和盐酸混合反应后的最高温度作为末温度 |
| C.除去CH3COOC2H5中的CH3COOH先加足量的饱和Na2CO3溶液再蒸馏 |
| D.能使湿润的KI淀粉试纸变蓝的气体一定是Cl2 |
B
试题分析:A. BaSO4尽管难溶,也有一定的溶解度。在溶液中存在沉淀溶解平衡:BaSO4(s)
 Ba2+(aq)+ SO42-(aq).,当向溶液中加入Na2CO3溶液时会发生反应:CO32-+Ba2+= BaCO3↓。产生难溶于水的BaCO3沉淀。破坏了BaSO4沉淀溶解平衡,促使其继续溶解。因此尽管Ksp(BaSO4)小于Ksp(BaCO3)也有一部分BaSO4沉淀转化为BaCO3沉淀。错误。B.在中和热测定的实验中,首先应该测定混合前酸、碱溶液的温度。然后将NaOH溶液和盐酸混合反应后的最高温度作为末温度,测定并记入数值。进行3次实验,取其平均值为反应的最终温度,然后利用Q=Cmt来计算反应热。正确。C.CH3COOH能与Na2CO3反应产生容易溶解于水的乙酸钠,不仅除去了杂质,还减小了CH3COOC2H5的溶解度。最后分液将混合物进行分离即得到纯净的CH3COOC2H5。错误。D.只要物质有强的氧化性,能把KI氧化为I2,都可以使能使湿润的KI淀粉试纸变蓝。所以该气体不一定是Cl2。错误。
Ba2+(aq)+ SO42-(aq).,当向溶液中加入Na2CO3溶液时会发生反应:CO32-+Ba2+= BaCO3↓。产生难溶于水的BaCO3沉淀。破坏了BaSO4沉淀溶解平衡,促使其继续溶解。因此尽管Ksp(BaSO4)小于Ksp(BaCO3)也有一部分BaSO4沉淀转化为BaCO3沉淀。错误。B.在中和热测定的实验中,首先应该测定混合前酸、碱溶液的温度。然后将NaOH溶液和盐酸混合反应后的最高温度作为末温度,测定并记入数值。进行3次实验,取其平均值为反应的最终温度,然后利用Q=Cmt来计算反应热。正确。C.CH3COOH能与Na2CO3反应产生容易溶解于水的乙酸钠,不仅除去了杂质,还减小了CH3COOC2H5的溶解度。最后分液将混合物进行分离即得到纯净的CH3COOC2H5。错误。D.只要物质有强的氧化性,能把KI氧化为I2,都可以使能使湿润的KI淀粉试纸变蓝。所以该气体不一定是Cl2。错误。
练习册系列答案
相关题目
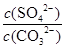 =
=
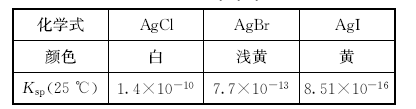
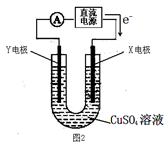
 Ag+(aq)+C1-(aq)
Ag+(aq)+C1-(aq)
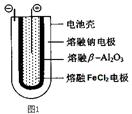
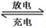 Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____: