题目内容
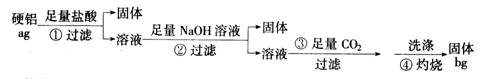
(16 分)某铝合金(硬铝)中含有铝、镁、铜、硅,为了测定该合金中铝的含量,有人设计了如下实验:
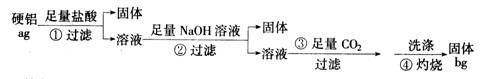
(1)补全上述①②③④各步反应的离子方程式
① Mg+2H+===Mg2++H2↑ , ___________________________
② _______________________, _______________________
Mg2++OH-===Mg(OH)2↓
③ ___________________________________
CO2+H20+ A102-===Al(OH)3↓+3HCO3-
④2A1(OH)3===Al203+H20
(2)该样品中铝的质量分数是( )
(3)第②步中加入Na0H溶液不足时,会使测定结果( )
第④步中的沉淀没有用蒸馏水洗涤时,会使测定结果( )
第④步对沉淀灼烧不充分时,会使测定结果( )
A.偏高 B.偏低 C.不影响
【答案】
(1)2Al+6H+ ===2 A13++3 H2↑ , H++OH-=== H20
A13++ 4OH—===A102-+2H20, CO2+ OH-=== HCO3—
(2)
(3)B,A,A
【解析】

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目