题目内容
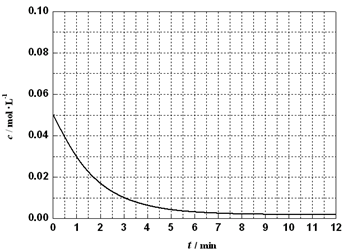
物质(t-BuNO)2在正庚烷或CCl4中均可以发生反应:(t-BuNO)2 2(t-BuNO)。在20℃时,向2 L正庚烷中加入(t-BuNO)2
1.0 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为75%(假设反应过程中溶液体积始终为2 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向2 L正庚烷中加入(t-BuNO)2
1.0 mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为75%(假设反应过程中溶液体积始终为2 L)。下列说法正确的是

A.反应在前10 min内的平均速率为ν(t-BuNO)=0.0375 mol·L-1·min-1
B.保持其他条件不变,若此时再向正庚烷反应体系中加入正庚烷,平衡向生成(t-BuNO)2的方向移动
C.保持其他条件不变,升高温度,(t-BuNO)2的平衡转化率大于75%,则其能量关系可用右图表示
D.保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率大于75%
【答案】
C
【解析】
试题分析:A、(t-BuNO)2的转化量为1.0×75%=0.75mol,ν(t-BuNO)=2(t-BuNO)2=2×0.75÷2÷10=0.075 mol·L-1·min-1,错误;B、体系中加入不反应的气体,反应物浓度不变,平衡不移动,错误;C、升高温度,反应物转化率增大平衡正向移动,反应吸热,正确;D、在正庚烷k=(1.5/2)2÷0.25/2=4.5大于在CCl4中平衡常数,平衡逆向移动,转化率减小,错误。
考点:考查化学平衡移动有关问题。

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
 2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50
mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是
2(t-BuNO)。在20℃时,向1 L正庚烷中加入(t-BuNO)2 0.50
mol,10 min时反应达平衡,此时(t-BuNO)2的平衡转化率为65%(假设反应过程中溶液体积始终为1 L)。下列说法正确的是


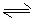 2(t-BuNO) 。
2(t-BuNO) 。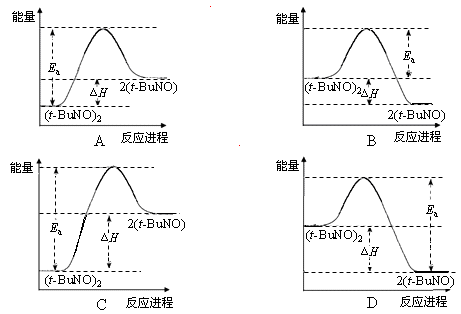
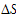 ____ 0(填“>”、“<”或“=”)。在 ________ (填“较高”或“较低”)温度下有利于该反应自发进行。
____ 0(填“>”、“<”或“=”)。在 ________ (填“较高”或“较低”)温度下有利于该反应自发进行。