题目内容
6.写出下列物质的电离方程式NaOH:NaOH=Na++OH-
H2SO4:H2SO4=2H++SO42-
NaCl:NaCl=Na++Cl-.
分析 强电解质在溶液中完全电离,电离方程式用“=”,氢氧化钠完全电离出钠离子和氢氧根离子,硫酸完全电离出氢离子和磷酸根离子,氯化钠完全电离出钠离子和硫酸根离子,据此写出其电离方程式.
解答 解:氢氧化钠是强碱,属于强电解质,在溶液中完全电离,其电离方程式为:NaOH=Na++OH-;
H2SO4是强酸,属于强电解质,在溶液中完全电离,其电离方程式为:H2SO4=2H++SO42-;
NaCl为强电解质,在溶液中完全电离出钠离子和氯离子,其电离方程式为:NaCl=Na++Cl-,
故答案为:NaOH=Na++OH-;H2SO4=2H++SO42-;NaCl=Na++Cl-.
点评 本题考查了电离方程式的书写,题目难度不大,注意掌握强弱电解质的概念及电离方程式的书写方法,试题注重了基础知识的考查,有利于培养学生的灵活应用能力.

练习册系列答案
相关题目
1.已知CN-(氢氰酸根离子)SCN-(硫氰酸根离子)和Cl-有相似之处:两个-CN原子团或两个-SCN原子团可分别构成氰分子(CN)2和硫氰分子(SCN)2.(CN)2和(SCN)2的性质和Cl2有性质有相似之处,且常温常压下是气体,下列物质间反应的化学方程式错误的是( )
| A. | 二氧化锰和HSCN溶液加热反应:MnO2+4HSCN$\frac{\underline{\;\;△\;\;}}{\;}$Mn(SCN)2+(SCN)2↑+2H2O | |
| B. | (CN)2和氢氧化钾溶液反应:(CN)2+2KOH═KCN+KCNO+H2O | |
| C. | 碘晶体投入HCN溶液中:I2+2HCN═2HI+(CN)2 | |
| D. | (SCN)2和水反应:(SCN)2+H2O?HSCN+HSCNO |
17.甲醛是居室装修中的主要污染物,它是一种高毒性的物质,被世界卫生组织确定为致癌和致畸形物质,是公认的变态反应源.甲醛分子中有3个σ键、一个π键,它们分别是( )
| A. | 碳原子的sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 | |
| B. | 碳原子的sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 | |
| C. | 碳原子的sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 | |
| D. | 碳、氧之间是sp2形成的σ键,碳、氧之间是未参加杂化的2p轨道形成的π键 | |
| E. | 碳、氧之间是sp2形成的σ键,碳、氢之间是未参加杂化的2p轨道形成的π键 |
1.有四位同学分别对四种溶液中所含的离子进行检测,结果如下,其中错误的是( )
| A. | Ca2+、HCO3-、Cl-、K+ | B. | OH-、CO32-、Cl-、K+ | ||
| C. | Ba2+、Na+、OH-、NO3- | D. | Cu2+、NO3-、OH-、Cl- |
11.下列反应所得溶液中一定只含一种溶质的是( )
| A. | 向AlCl3溶液中滴入NaOH溶液 | |
| B. | 向NaOH溶液中通入SO2气体 | |
| C. | 向浓硝酸中加入过量铜粉 | |
| D. | 向MgCl2、H2SO4的混合液中滴入过量Ba(OH)2溶液 |
15.可逆反应:3X(g)?3Y(?)+Z(?)△H<0,随着温度的降低,气体的平均相对分子质量有变小的趋势,则下列判断正确的是( )
| A. | Y和Z可能都是气体 | B. | Y和Z可能都是固体 | ||
| C. | 若Z为固体,则Y一定是气体 | D. | Y和Z一定是气体 |
16.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 铁和稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 碳酸氢钠溶液中滴入NaOH溶液:HCO${\;}_{3}^{-}$+OH-═H2O+CO2↑ | |
| D. | 硫酸溶液中加入氢氧化钡溶液:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ |
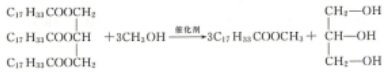 .
.
 ,DMCCH3OCOOCH3.
,DMCCH3OCOOCH3.