��Ŀ����
16������Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���д���пհף�
��1������ЩԪ���У���ѧ��������õ���Ar����Ԫ�ط��ţ�
��2���ڢۢ�����Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳��ΪCl��N��O ����Ԫ�ط��ţ�
��3��������������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽHClO4��������ǿ�Ļ�����������������أ�
��4��Ԫ�آݵ���������Ԫ�آܵ�����������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽΪ��Al2O3+2NaOH=2NaAlO2+H2O
��5��Ԫ�آ͢��γɵ���̬�⻯����ȶ���HCl���ѧʽ�����÷���ʽ��˵��Ԫ�آߵķǽ����ԱȢķǽ���ǿ����ʵCl2+H2S=S��+2HCl��һ������������ʽ���ɣ�
��6����ʾ������γɵĻ�����ĵ���ʽ
 ��д������һ����;���ܼ��������ȣ�
��д������һ����;���ܼ��������ȣ�
���� ��Ԫ�������ڱ���λ��֪����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK��
��1��ϡ�����廯ѧ��������ã�
��2��ͬ�����������ԭ�Ӱ뾶��С�����Ӳ�Խ��ԭ�Ӱ뾶Խ��
��3��������������ˮ�����У�������ǿ�Ļ������Ǹ����ᣬ����Ԫ����K�Ľ�������ǿ�����������ؼ�����ǿ��
��4�����������������Ʒ�Ӧ����ƫ��������ˮ��
��5���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ����������õ���֮����û��Ƚ�����֤��
��6����ʾ������γɵĻ�����ΪCCl4�����������ܼ��������ȣ�
��� �⣺��Ԫ�������ڱ���λ��֪����ΪC����ΪN����ΪO����ΪNa����ΪAl����ΪS����ΪCl����ΪAr����ΪK��
��1��ϡ������Arԭ�������Ϊ�ȶ��ṹ����ѧ��������ã��ʴ�Ϊ��Ar��
��2��ͬ�����������ԭ�Ӱ뾶��С�����Ӳ�Խ��ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶��Cl��N��O���ʴ�Ϊ��Cl��N��O��
��3��������������ˮ�����У�������ǿ�Ļ�������HClO4������Ԫ����K�Ľ�������ǿ�����������ؼ�����ǿ���ʴ�Ϊ��HClO4���������أ�
��4�����������������Ʒ�Ӧ����ƫ��������ˮ����Ӧ����ʽΪ��Al2O3+2NaOH=2NaAlO2+H2O���ʴ�Ϊ��Al2O3+2NaOH=2NaAlO2+H2O��
��5���ǽ�����S��Cl���ǽ�����Խǿ����Ӧ�⻯��Խ�ȶ������⻯���ȶ���H2S��HCl���������õ���֮����û��Ƚ�����֤����Ӧ����ʽΪCl2+H2S=S��+2HCl�ȣ�
�ʴ�Ϊ��HCl��Cl2+H2S=S��+2HCl��
��6����ʾ������γɵĻ�����ΪCCl4������ʽΪ �����������ܼ��������ȣ��ʴ�Ϊ��
�����������ܼ��������ȣ��ʴ�Ϊ�� �����ܼ��������ȣ�
�����ܼ��������ȣ�
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɵĹ�ϵ����Ŀ�ѶȲ���ע������ԡ��ǽ�����ǿ���Ƚ�ʵ����ʵ��

 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�| A�� | �ӵ��ξ��ǡ�I2+NaCl�� | B�� | �ӵ��ξ���NaCl�м���KI | ||
| C�� | �ӵ�����NaCl�м�������KIO3 | D�� | �ӵ��ξ��Ǵ�KIO3 |
| A�� | ��ռ�����һ����� | B�� | ����ԭ��������� | ||
| C�� | ��������������� | D�� | ������������� |
| A�� | FeS | B�� | FeCl3 | C�� | Fe3O4 | D�� | FeCl2 |
| A�� | 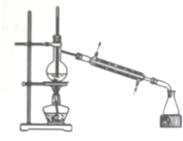 ʯ�ͷ��� | B�� | 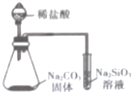 �ȽϷǽ����ԣ�Cl��C��Si | ||
| C�� |  �γ�ԭ��� | D�� |  ���ȷ�Ӧ |
| ���ϱ� | ���ƺ��Ρ������ |
| ������ | 20��40mg/kg |
| ��������֤�� | ���������֣�1999����001�� |
| ��װ���� | ����� |
| ���ط��� | �ܷ⡢�ܹ⡢���� |
| ʳ�÷��� | ���ʱ����ʳƷ��������� |
��2��ʳ���мӵ⣬���ָ����Ԫ�أ�����ʡ������������Ԫ�ء��������е�Ԫ�صĻ��ϼ�Ϊ+5��
��3�����ݺ����ε�ʳ�÷������Ʋ��Ԫ�صĻ�ѧ���ʣ������������ʱ���ֽ⣮
 ��Dԭ�ӵ�ԭ�ӽṹʾ��ͼΪ
��Dԭ�ӵ�ԭ�ӽṹʾ��ͼΪ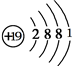 ��C+���ӵĽṹʾ��ͼΪ
��C+���ӵĽṹʾ��ͼΪ ��
�� ��1���������ѧ��FulvioCacace�Ȼ���˼��������о������N4���ӣ�N4���ӽṹ��ͼ��ʾ����֪����1mol N-N����167kJ����������1mol N��N�ų�942kJ������������Ϣ�����ݣ�����1molN4����ת��ΪN2����ġ�H=-882 kJ•mol-1
��1���������ѧ��FulvioCacace�Ȼ���˼��������о������N4���ӣ�N4���ӽṹ��ͼ��ʾ����֪����1mol N-N����167kJ����������1mol N��N�ų�942kJ������������Ϣ�����ݣ�����1molN4����ת��ΪN2����ġ�H=-882 kJ•mol-1