题目内容
11.2升由甲烷、乙烷、甲醛组成的混合气体,完全燃烧后生成15.68升CO2(气体体积均在同温同压下测定),混合气体中乙烷的体积百分含量为
| A.20% | B.40% | C.60% | D.80% |
B
试题分析:n(气体)=11.2L÷22.4L/mol=0.5mol。n(CO2)= 15.68L÷22.4L/mol=0.7mol。由于甲烷、甲醛分子中都只含有一个C原子,所以假设它们二者的物质的量为x,乙烷的物质的量为y.则根据题意可得x+y=0.5;x+2y=0.7.解得x=0.3mol;y=0.2mol。对于气体来说,体积比为气体的物质的量的比,因此混合气体中乙烷的体积百分含量为(0.2÷0.5)×100%=40%。因此选项是B。

练习册系列答案
相关题目
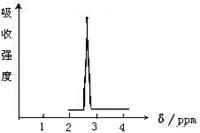
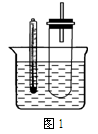
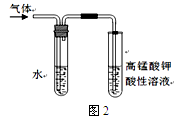
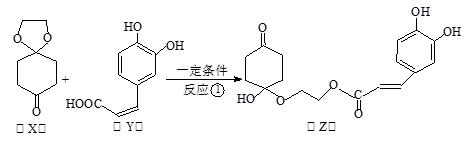
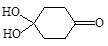 )分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N(分子式为C6H8O2),则N的结构简式为 (已知烯醇式不稳定,会发生分子重排,例如:
)分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N(分子式为C6H8O2),则N的结构简式为 (已知烯醇式不稳定,会发生分子重排,例如: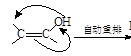
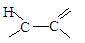 )。
)。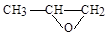 )发生类似反应①的反应,其生成物的结构简式为 (写一种);Y的同分异构体很多种,其中有苯环、苯环上有三个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有 种。
)发生类似反应①的反应,其生成物的结构简式为 (写一种);Y的同分异构体很多种,其中有苯环、苯环上有三个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有 种。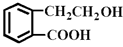 的有机物可以通过不同的反应得到下列四种物质:
的有机物可以通过不同的反应得到下列四种物质: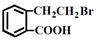 ②
②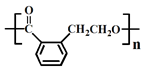 ③
③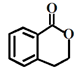 ④
④