��Ŀ����
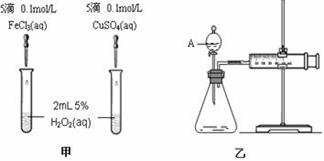
Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч����ij��ѧ�о�С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣��ش�������⣺

��1�����Է�������ͼ��ͨ���۲� �����ԱȽϵó����ۡ���ͬѧ�����Cu SO4��ΪCuCl2��Ϊ�������������� ������������
��2��������������ͼ����ʾ��ʵ��ʱ��������40mL����Ϊ����������Ӱ��ʵ������ؾ��Ѻ��ԡ�ͼ������A������Ϊ ��ʵ������Ҫ������������ �� �� ��
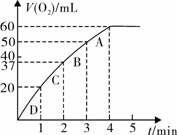
��3������0.10 mol MnO2��ĩ��50 mL H2O2��Һ�У��ڱ�״���·ų�����������ʱ��Ĺ�ϵ��ͼ��ʾ��
��ʵ��ʱ�ų������������� mL��
��A��B��C��D���㷴Ӧ���ʿ�����˳��Ϊ_____��____��____��____��
�۽��ͷ�Ӧ���ʱ仯��ԭ�� ��
��1����λʱ���ڲ������ݵĿ����� ���������Ӳ�ͬ��ʵ��ĸ��ţ����Ʊ�����������
��2����Һ©���� ����40mL���������ʱ��
��3���� 60 �� �� D>C>B>A�� �����ŷ�Ӧ�Ľ��У���Ӧ��Ũ�ȼ�С����Ӧ���ʼ���
����������1��Ҫ�ȽϷ�Ӧ�Ŀ���������ͨ���۲쵥λʱ���ڲ������ݵĿ�����ʵ�֡�Ϊ�����������ӵIJ�ͬ��ʵ��ĸ��ţ������Ȼ�ͭ��������
��2�����������Ľṹ��֪���Ƿ�Һ©��������ͨ������ ����40mL���������ʱ�����ȽϷ�Ӧ���ʴ�С��
��3������ͼ���֪������Ӧ�в���60ml����ʱ������Ͳ��ٷ����仯��ʵ������������ʱ60ml�������������������֪��A��B��C��D���㷴Ӧ���ʿ�����˳��Ϊ D>C>B>A���������ŷ�Ӧ�Ľ��У���Ӧ��Ũ����С����Ӧ����������

 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�Ϊ�Ƚ�Fe3+��Cu2+��H2O2�ֽ�Ĵ�Ч�����ס���ͬѧ�ֱ��������ͼһ��ͼ����ʾ��ʵ�顣
���� (1) H2O2�ֽ�Ļ�ѧ����ʽΪ �������������������������������������� ��
 |
ͼһ�������������������������������� ͼ��
��2��ͼһ��ʾʵ���ܶ���˵����Ӧ������������ _______________________________;
��ͼ����ʾʵ����˵����Ӧ������������____________________________________��
��3���� ��H2O2��H2SO4�Ļ����Һ���ܽ�ӡˢ��·�������ĩ�е�ͭ����֪��
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g)�� ��H= �� 64.39 kJ/mol
2H2O2(l)=2H2O(l) + O2(g)������ ��H= ��196. 46 kJ/mol
���� H2(g) + 1/2O2(g) = H2O(l)������ ��H= ��285. 84 kJ/mol
��H2SO4��Һ��Cu��H2O2��Ӧ����Cu2+ ��H2O���Ȼ�ѧ����ʽΪ��
�� �������������������������������������������������������������������� ��
�� �� ��������������ͬ��ӡˢ��·��Ľ�����ĩ��10% H2O2��3 .0 mol/L H2SO4�Ļ�
���� ����Һ��������ò�ͬ�¶���ͭ��ƽ���ܽ����ʣ����±�����
�¶ȣ��棩 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
ͭƽ���ܽ����ʡ��� ����10��3 mol��L��1��min��1�� | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
���¶ȸ���40��ʱ��ͭ��ƽ���ܽ��������ŷ�Ӧ�¶����߶��½�������Ҫԭ��
������������������������������������������������������������������ ��