题目内容
标准状况下有①6.72LCH4②3.01×1023个HCl③13.6gH2S④0.2molNH3,下列对四种气体的关系从小到大表示不正确的是
| A.体积 ④<①<③<② | B.密度 ①<④<③<② |
| C.质量 ④<①<③<② | D.氢原子数 ④<②<③<① |
D
试题分析:根据题意可知,甲烷、氯化氢、H2S的物质的量分别是6.72L÷22.4L/mol=0.3mol、
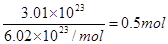 、13.6g÷34g/mol=0.4mol。根据阿伏加德罗定律可知,气体的体积大小关系是④<①<③<②,A正确;在相同条件下,气体的密度之比是相对分子质量之比,B正确;甲烷的质量是4.8g、氯化氢的质量是18.25g、氨气的质量是3.4g,所以质量关系是④<①<③<②,C正确。氢原子的物质的量分别是1.2mol、0.5mol、0.8mol、0.6mol,则氢原子数 ②<④<③<①,D不正确,答案选D。
、13.6g÷34g/mol=0.4mol。根据阿伏加德罗定律可知,气体的体积大小关系是④<①<③<②,A正确;在相同条件下,气体的密度之比是相对分子质量之比,B正确;甲烷的质量是4.8g、氯化氢的质量是18.25g、氨气的质量是3.4g,所以质量关系是④<①<③<②,C正确。氢原子的物质的量分别是1.2mol、0.5mol、0.8mol、0.6mol,则氢原子数 ②<④<③<①,D不正确,答案选D。点评:该题是中等难度的试题,试题综合性强,在注重对基础知识考查的同时,更侧重对学生能力的培养。该题学生需要注意的是在进行物质的量的有关计算时,关键是熟练应用几个关系式
 、n=m/M、
、n=m/M、 、
、 ,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
,特别还要注意气体摩尔体积的使用条件,即只能适用于气体,且只有在标准状况下,气体的摩尔体积才是22.4L/mol。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目