题目内容
铁黄是一种重要的颜料,化学式为Fe2O3?xH2O,广泛用于涂料、橡胶、塑料、文教用品等工业.实验室模拟工业利用硫酸渣(含Fe2O3及少量的CaO、MgO等)和黄铁矿粉(主要成分为FeS2)制备铁黄的流程如图:
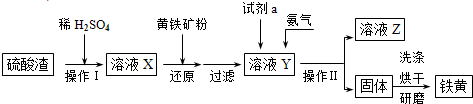
(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是______、______.
(2)试剂a最好选用______(供选择使用的有:铝粉、空气、浓HNO3);其作用是______.
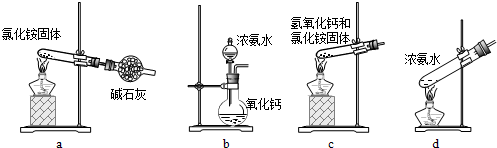
(3)上述步骤中需用到氨气.下列装置可用于实验室制氨气的是______(填序号).

(4)检验溶液Z中含有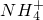 的方法是______.
的方法是______.
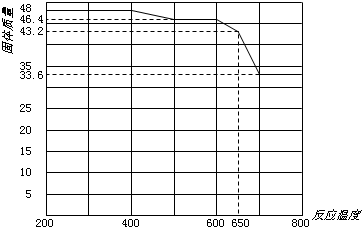
(5)查阅资料知,在不同温度下Fe2O3被CO还原,产物可能为Fe3O4、FeO或Fe,固体质量与反应温度的关系如下图所示.
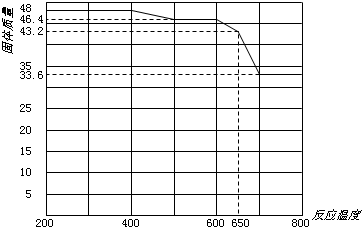
根据图象推断670℃时Fe2O3还原产物的化学式为______,并设计一个简单的实验,证明该还原产物的成分(简述实验操作、现象和结论).______.仪器自选.可供选择的试剂:稀H2SO4、稀盐酸、H2O2溶液、NaOH溶液、KSCN溶液.
解:(1)操作Ⅰ与操作Ⅱ中都用到玻璃棒,玻璃棒在两种操作中的作用分别是,操作Ⅰ是利用玻璃棒加速硫酸渣的溶解,操作Ⅱ是过滤实验操作,玻璃棒是起到引流作用;
故答案为:搅拌加速溶解(或搅拌加速反应);引流;
(2)依据流程分析,试剂a是用来氧化亚铁离子的主要,但选择氧化剂不能引入新的杂质,铝粉引入新的杂质,浓硝酸做氧化剂会产生污染气体,最好选择空气做氧化剂氧化亚铁离子,不会引入新的杂质,不污染环境;
故答案为:空气; 作氧化剂,将Fe2+氧化为Fe3+;
(3)a、加热氯化铵分解后生成氨气和氯化氢会在试管口重新生成氯化铵;不能制的氨气,故a不能;
b、氨水滴入氧化钙固体,氧化钙会和水反应生成氢氧化钙放热,使一水合氨分解生成氨气;故b符合;
c、氢氧化钙和氯化铵固体加热时需要试管口略向下倾斜,装置中加热会使生成的水倒流到试管底部炸裂试管;故c不选;
d、加热浓氨水会分解生成氨气,可以制取氨气;故d符合;
故答案为:bd;
(4)溶液Z中含NH4+的实验方法是利用铵根离子和氢氧根离子结合反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝;取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+;
故答案为:取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+;
(5)CO还原氧化铁的还原产物为可能Fe3O4,FeO和Fe.Fe2O3加热温度可达到500℃~600℃,质量由46.4g减少为45g,还原产物为Fe3O4;650℃~700℃时,质量由43.2g减少较大,还原产物为FeO,为验证还原产物,在适量待检物中加入稀H2SO4至完全溶解,再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,可说明还原产物为FeO;
故答案为:FeO;取少量还原产物置于试管中,加入过量稀硫酸(或稀盐酸),固体完全溶解且无气泡产生;再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,证明还原产物为FeO;
分析:(1)操作Ⅰ是利用玻璃棒加速硫酸渣的溶解,操作Ⅱ是过滤实验操作,玻璃棒是起到引流作用;
(2)试剂a是把亚铁离子氧化为铁离子;选择氧化剂不能引入新的杂质,不能产生污染物;
(3)a、加热氯化铵分解后生成氨气和氯化氢会在试管口重新生成氯化铵;
b、氨水滴入氧化钙固体,氧化钙会和水反应生成氢氧化钙放热,使一水合氨分解生成氨气;
c、氢氧化钙和氯化铵固体加热时需要试管口略向下倾斜;
d、加热浓氨水会分解生成氨气;
(4)溶液Z主要是铵盐,依据铵根离子检验方法分析判断;
(5)CO还原氧化铁的还原产物为可能Fe3O4,FeO和Fe.Fe2O3加热温度可达到500℃~600℃,质量由46.4g减少为45g,还原产物为Fe3O4;650℃~700℃时,质量由43.2g减少较大,还原产物为FeO,利用亚铁离子的还原性来设计实验.
点评:本题考查了物质提纯和分离的方法分析,实验设计,物质性质的综合应用,图象分析判断计算应用,题目难度中等.
故答案为:搅拌加速溶解(或搅拌加速反应);引流;
(2)依据流程分析,试剂a是用来氧化亚铁离子的主要,但选择氧化剂不能引入新的杂质,铝粉引入新的杂质,浓硝酸做氧化剂会产生污染气体,最好选择空气做氧化剂氧化亚铁离子,不会引入新的杂质,不污染环境;
故答案为:空气; 作氧化剂,将Fe2+氧化为Fe3+;
(3)a、加热氯化铵分解后生成氨气和氯化氢会在试管口重新生成氯化铵;不能制的氨气,故a不能;
b、氨水滴入氧化钙固体,氧化钙会和水反应生成氢氧化钙放热,使一水合氨分解生成氨气;故b符合;
c、氢氧化钙和氯化铵固体加热时需要试管口略向下倾斜,装置中加热会使生成的水倒流到试管底部炸裂试管;故c不选;
d、加热浓氨水会分解生成氨气,可以制取氨气;故d符合;
故答案为:bd;
(4)溶液Z中含NH4+的实验方法是利用铵根离子和氢氧根离子结合反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝;取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+;
故答案为:取少量溶液Z置于试管中,滴加过量浓NaOH溶液并微热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝色,证明含有NH4+;
(5)CO还原氧化铁的还原产物为可能Fe3O4,FeO和Fe.Fe2O3加热温度可达到500℃~600℃,质量由46.4g减少为45g,还原产物为Fe3O4;650℃~700℃时,质量由43.2g减少较大,还原产物为FeO,为验证还原产物,在适量待检物中加入稀H2SO4至完全溶解,再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,可说明还原产物为FeO;
故答案为:FeO;取少量还原产物置于试管中,加入过量稀硫酸(或稀盐酸),固体完全溶解且无气泡产生;再向其中滴加KSCN溶液,溶液不变色;最后滴加H2O2溶液,溶液变红色,证明还原产物为FeO;
分析:(1)操作Ⅰ是利用玻璃棒加速硫酸渣的溶解,操作Ⅱ是过滤实验操作,玻璃棒是起到引流作用;
(2)试剂a是把亚铁离子氧化为铁离子;选择氧化剂不能引入新的杂质,不能产生污染物;
(3)a、加热氯化铵分解后生成氨气和氯化氢会在试管口重新生成氯化铵;
b、氨水滴入氧化钙固体,氧化钙会和水反应生成氢氧化钙放热,使一水合氨分解生成氨气;
c、氢氧化钙和氯化铵固体加热时需要试管口略向下倾斜;
d、加热浓氨水会分解生成氨气;
(4)溶液Z主要是铵盐,依据铵根离子检验方法分析判断;
(5)CO还原氧化铁的还原产物为可能Fe3O4,FeO和Fe.Fe2O3加热温度可达到500℃~600℃,质量由46.4g减少为45g,还原产物为Fe3O4;650℃~700℃时,质量由43.2g减少较大,还原产物为FeO,利用亚铁离子的还原性来设计实验.
点评:本题考查了物质提纯和分离的方法分析,实验设计,物质性质的综合应用,图象分析判断计算应用,题目难度中等.

练习册系列答案
相关题目





 的方法是
。
的方法是
。


 的方法是______________。
的方法是______________。