题目内容
NA代表阿伏加德罗常数,下列说法正确的是
- A.5.6g铁与足量的盐酸反应转移的电子数为0.3NA
- B.100mL2mol/L的盐酸与醋酸的溶液中氢离子数均为0.2NA
- C.1molFeCl3和水反应制得的氢氧化铁胶体所含胶粒数为NA
- D.常温常压下,28g的一氧化碳气和氮气的混合气中含有原子数为2NA
D
分析:A、铁与盐酸反应生成氯化亚铁和氢气,铁由0价升高为+2价,根据铁计算注意的电子数.
B、氯化氢为强电解质完全电离,醋酸为弱电解质部分电离.
C、氢氧化铁胶体微粒是由许多个氢氧化铁“分子”聚在一起形成的.
D、一氧化碳气和氮气的摩尔质量都是28g/mol,所以平均摩尔质量为28g/mol,根据n= 混合气体的总的物质的量,一氧化碳气和氮气为双原子分子,再根据N=nNA计算原子数目.
混合气体的总的物质的量,一氧化碳气和氮气为双原子分子,再根据N=nNA计算原子数目.
解答:A、5.6g铁的物质的量为0.1mol,铁与盐酸反应生成氯化亚铁和氢气,铁由0价升高为+2价,转移的电子数为0.1mol×2×NAmol-1=0.2NA,故A错误;
B、氯化氢为强电解质完全电离,2mol/L的盐酸中氢离子浓度为2mol/L,100ml2mol/L的盐酸中氢离子数目为0.1L×2mol/L×NAmol-1=0.2NA,醋酸为弱电解质部分电离,2mol/L醋酸的溶液中氢离子浓度远小于2mol/L,100ml2mol/L的醋酸中氢离子数目远小于0.1L×2mol/L×NAmol-1=0.2NA,故B错误;
C、1mol氯化铁不能完全水解,胶粒是一种微粒的集合体,胶粒数应远远小于NA,故C错误;
D、一氧化碳气和氮气的摩尔质量都是28g/mol,所以平均摩尔质量为28g/mol,混合气体的总的物质的量为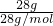 =
=
1mol,一氧化碳气和氮气为双原子分子,含有的原子数目为1mol×2×NAmol-1=2NA,故D正确.
故选:D.
点评:考查常用化学计量的有关计算,难度不大,注意基础知识的理解掌握.
分析:A、铁与盐酸反应生成氯化亚铁和氢气,铁由0价升高为+2价,根据铁计算注意的电子数.
B、氯化氢为强电解质完全电离,醋酸为弱电解质部分电离.
C、氢氧化铁胶体微粒是由许多个氢氧化铁“分子”聚在一起形成的.
D、一氧化碳气和氮气的摩尔质量都是28g/mol,所以平均摩尔质量为28g/mol,根据n=
 混合气体的总的物质的量,一氧化碳气和氮气为双原子分子,再根据N=nNA计算原子数目.
混合气体的总的物质的量,一氧化碳气和氮气为双原子分子,再根据N=nNA计算原子数目.解答:A、5.6g铁的物质的量为0.1mol,铁与盐酸反应生成氯化亚铁和氢气,铁由0价升高为+2价,转移的电子数为0.1mol×2×NAmol-1=0.2NA,故A错误;
B、氯化氢为强电解质完全电离,2mol/L的盐酸中氢离子浓度为2mol/L,100ml2mol/L的盐酸中氢离子数目为0.1L×2mol/L×NAmol-1=0.2NA,醋酸为弱电解质部分电离,2mol/L醋酸的溶液中氢离子浓度远小于2mol/L,100ml2mol/L的醋酸中氢离子数目远小于0.1L×2mol/L×NAmol-1=0.2NA,故B错误;
C、1mol氯化铁不能完全水解,胶粒是一种微粒的集合体,胶粒数应远远小于NA,故C错误;
D、一氧化碳气和氮气的摩尔质量都是28g/mol,所以平均摩尔质量为28g/mol,混合气体的总的物质的量为
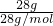 =
=1mol,一氧化碳气和氮气为双原子分子,含有的原子数目为1mol×2×NAmol-1=2NA,故D正确.
故选:D.
点评:考查常用化学计量的有关计算,难度不大,注意基础知识的理解掌握.

练习册系列答案
相关题目