题目内容
100g CaCO3与30g SiO2的混合物加强热,使之充分反应。请计算得到气体的体积为多少(标准状况)?
22.4 L
方法1(常规法):二者混合加强热发生的反应为:CaCO3 + SiO2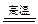 CaSiO3 + CO2↑,特别要注意的是:30g SiO2完全反应只消耗50g CaCO3,剩余的 CaCO3还要单独分解,又生成一部分CO2。
CaSiO3 + CO2↑,特别要注意的是:30g SiO2完全反应只消耗50g CaCO3,剩余的 CaCO3还要单独分解,又生成一部分CO2。
解:CaCO3+ SiO2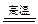 CaSiO3+ CO2↑
CaSiO3+ CO2↑
100 g 60 g 22.4 L
50 g 30 g 11.2 L
在第一步反应中,生成CO2 11.2 L,剩余CaCO3100 g-50 g=50 g
CaCO3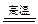 CaO +CO2↑
CaO +CO2↑
100 g 22.4 L
50 g 11.2 L
在第二步反应中,又生成CO2 11.2 L。因此,得到气体的体积共为22.4 L。
方法2(思维转换):不妨把思维转换一下,认为在高温下CaCO3先分解,然后分解生成的氧化钙再与SiO2反应:CaCO3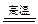 CaO + CO2↑;SiO2+CaO
CaO + CO2↑;SiO2+CaO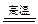 CaSiO3。根据第一步反应容易计算得生成气体的体积为22.4 L。
CaSiO3。根据第一步反应容易计算得生成气体的体积为22.4 L。
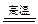 CaSiO3 + CO2↑,特别要注意的是:30g SiO2完全反应只消耗50g CaCO3,剩余的 CaCO3还要单独分解,又生成一部分CO2。
CaSiO3 + CO2↑,特别要注意的是:30g SiO2完全反应只消耗50g CaCO3,剩余的 CaCO3还要单独分解,又生成一部分CO2。解:CaCO3+ SiO2
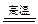 CaSiO3+ CO2↑
CaSiO3+ CO2↑100 g 60 g 22.4 L
50 g 30 g 11.2 L
在第一步反应中,生成CO2 11.2 L,剩余CaCO3100 g-50 g=50 g
CaCO3
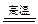 CaO +CO2↑
CaO +CO2↑100 g 22.4 L
50 g 11.2 L
在第二步反应中,又生成CO2 11.2 L。因此,得到气体的体积共为22.4 L。
方法2(思维转换):不妨把思维转换一下,认为在高温下CaCO3先分解,然后分解生成的氧化钙再与SiO2反应:CaCO3
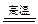 CaO + CO2↑;SiO2+CaO
CaO + CO2↑;SiO2+CaO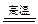 CaSiO3。根据第一步反应容易计算得生成气体的体积为22.4 L。
CaSiO3。根据第一步反应容易计算得生成气体的体积为22.4 L。
练习册系列答案
相关题目
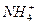 +Cl-,NH4Cl属于盐
+Cl-,NH4Cl属于盐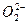 ====O2↑+4OH-
====O2↑+4OH- ====3BaSO4↓+2Al(OH)3↓
====3BaSO4↓+2Al(OH)3↓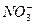 ====Cu2++2NO↑+H2O
====Cu2++2NO↑+H2O
 ZnCl2+ZnI2,ICl+H2O
ZnCl2+ZnI2,ICl+H2O 2CuO B.Fe+S
2CuO B.Fe+S