题目内容
【题目】KClO4具有强氧化性,可用作炸药等。实验室由KClO3分解制备KClO4的流程如图:

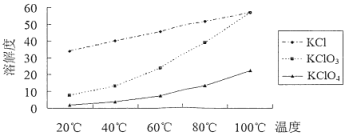
已知KClO3熔融易烧结,400℃以上分解放出氧气,各物质溶解度如下图。下列说法不正确的是
A.实验室制备KClO4的原理为![]()
B.趁热过滤的目的是除去KCl
C.操作①是冷却结晶、过滤、洗涤,操作②是重结晶
D.加热分解时,如果温度过高会使产率下降
【答案】B
【解析】
根据流程:KClO3加热至100℃使之熔融,加热30min分解:4KClO3 ![]() 3KClO4+KCl,冷却,固体为KClO4,含有KCl、KClO3,加水溶解煮沸,为减少KClO3结晶析出损失,趁热过滤,将滤液冷却结晶、过滤、洗涤,得到主要含有KClO4,少量的KCl、KClO3,重结晶得到、干燥得到产品,据此分析作答。
3KClO4+KCl,冷却,固体为KClO4,含有KCl、KClO3,加水溶解煮沸,为减少KClO3结晶析出损失,趁热过滤,将滤液冷却结晶、过滤、洗涤,得到主要含有KClO4,少量的KCl、KClO3,重结晶得到、干燥得到产品,据此分析作答。
A.实验室由KClO3分解制备KClO4,根据化合价有升有降,还有KCl生成,反应为:4KClO3![]() 3KClO4+KCl,故A正确;
3KClO4+KCl,故A正确;
B.由流程可知趁热过滤后KClO4在滤液中,由图KCl的溶解度比KClO4大,故KCl也在滤液中,故B错误;
C.KClO4的溶解度随温度的升高而增大,操作①后得到粗产品,故从滤液中得到产品为冷却结晶、过滤、洗涤,经过操作②粗产品得到精产品,由图可知,产品与杂质的溶解度随温度的变化较大,故为重结晶,故C正确;
D.加热分解时,如果温度过高,KClO3分解放出氧气,2KClO3![]() 3O2↑+2KCl,产率下降,故D正确;
3O2↑+2KCl,产率下降,故D正确;
故答案为B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目