题目内容
4.相同质量的下列物质,含分子数目最多的是( )| A. | H2 | B. | CO2 | C. | N2 | D. | NH3 |
分析 根据n=$\frac{m}{M}$判断物质的量大小,由N=nNA可知,物质的量越大,含有的分子数目越多.
解答 解:根据n=$\frac{m}{M}$可知,相同质量时,摩尔质量越小,物质的量越大,而物质的量越大,含有的分子数目越多,选项中氢气的摩尔质量最小,故相同质量时,氢气含有的分子数目最多,故选:A.
点评 本题考查物质的量有关计算,比较基础,注意对公式的理解与灵活应用,有利于基础知识的巩固.

练习册系列答案
相关题目
14.葡萄糖酸钙是一种可促进骨骼生长的营养物质.葡萄糖酸钙可通过以下反应制得:
CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
实验流程如下:
葡萄糖溶液滴加3%溴水/55℃:①过量CaCO3/70℃②趁热过滤 ③乙醇 ④悬浊液
抽滤⑤洗涤⑥干燥⑦Ca(C6H11O7)2
葡萄糖溶液$→_{①}^{滴加3%溴水/55℃}$ $\underset{\stackrel{过量CaC{O}_{3}/70℃}{→}}{②}$ $→_{③}^{趁热过滤}$ $→_{④}^{乙醇}$ 悬浊液$→_{⑤}^{抽滤}$ $→_{⑥}^{洗涤}$$→_{⑦}^{干燥}$Ca(C6H11O7)2
请回答下列问题:
(1)第 ①步中溴水氧化葡萄糖时,下列装置最合适的是B(填序号).
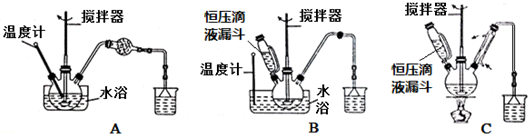
(2)第 ②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率,且过量的碳酸钙易除去.
(3)本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应制得葡萄糖酸钙.
(4)第 ③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤或损失产品.
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2OH(CHOH)4COONa+Cu2O↓+3H2O.
CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
葡萄糖溶液滴加3%溴水/55℃:①过量CaCO3/70℃②趁热过滤 ③乙醇 ④悬浊液
抽滤⑤洗涤⑥干燥⑦Ca(C6H11O7)2
葡萄糖溶液$→_{①}^{滴加3%溴水/55℃}$ $\underset{\stackrel{过量CaC{O}_{3}/70℃}{→}}{②}$ $→_{③}^{趁热过滤}$ $→_{④}^{乙醇}$ 悬浊液$→_{⑤}^{抽滤}$ $→_{⑥}^{洗涤}$$→_{⑦}^{干燥}$Ca(C6H11O7)2
请回答下列问题:
(1)第 ①步中溴水氧化葡萄糖时,下列装置最合适的是B(填序号).

(2)第 ②步充分反应后CaCO3固体需有剩余,其目的是提高葡萄糖酸的转化率,且过量的碳酸钙易除去.
(3)本实验中不宜用CaCl2替代CaCO3,理由是氯化钙难以与葡萄糖酸直接反应制得葡萄糖酸钙.
(4)第 ③步需趁热过滤,其原因是葡萄糖酸钙冷却后会结晶析出,如不趁热过滤或损失产品.
(5)葡萄糖溶液与新制Cu(OH)2悬浊液反应的化学方程式为CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH2OH(CHOH)4COONa+Cu2O↓+3H2O.
16.下列顺序不正确的是( )
| A. | 热稳定性:HCl>HBr>HI | |
| B. | 微粒的半径:Cl->Na+>Mg2+ | |
| C. | 离子的还原性:S2->Cl->F- | |
| D. | 电离程度(同温度同浓度溶液中):HCl>CH3COOH>NaHCO3 |
13.下列状态时,能够导电的电解质是( )
| A. | 石墨 | B. | 熔融态的氯化钠 | C. | 硫酸铜溶液 | D. | 干冰 |
 .
.
 .
.
 $\stackrel{过氧化物}{→}$
$\stackrel{过氧化物}{→}$ (R,R′代表烃基)
(R,R′代表烃基) .
. .
.