题目内容
具有下列电子层结构的原子,其相应元素一定属于同一主族的是
| A.3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子 |
| B.3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子 |
| C.最外层电子排布为1s2的原子和最外层电子排布为2s22p6的原子 |
| D.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子 |
B
试题分析:A、p轨道上有2个未成对电子,可能为2或4,不能确定元素的种类,则不一定为同一主族,故A错误;B、p轨道上只有1个空轨道,应含有2个电子,应为ⅣA族元素,故B正确;C、最外层电子排布为1s2的为He,属于0族元素。最外层电子排布为2s22p6的原子为Ne,属于0族元素,所以C错误;D、最外层电子排布为1s2的原子为He,属于0族元素。最外层电子排布为2s2的原子Be元素,属于主族元素,故D错误,答案选B。

练习册系列答案
相关题目
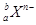 ,下列说法正确的是
,下列说法正确的是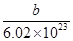 g
g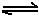 2X(g);△H ="-92.4" kJ·mol-1,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有 。
2X(g);△H ="-92.4" kJ·mol-1,在适当的催化剂和恒温恒压条件下反应,下列说法正确的有 。