题目内容
【题目】实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.
【方案一】:沉淀法.利用化学反应把HCO3﹣、CO32﹣完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中ω(Na2CO3).
(1)量取100mL配制好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO3﹣、CO32﹣完全转化为沉淀,应选用的试剂是 (填编号).
A.CaCl2溶液 B.MgSO4溶液 C.NaCl溶液 D.Ba(OH)2溶液
(2)将所得沉淀充分干燥,称量沉淀的质量为mg,由此可以计算ω(Na2CO3).如果此步中,沉淀未干燥充分就称量,则测得ω(Na2CO3) (填“偏大”、“偏小“或“无影响”).
【方案二】:量气法.量取10.00mL配制好的溶液与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃、1.01×105Pa)的体积,由此计算混合物中ω(Na2CO3)。
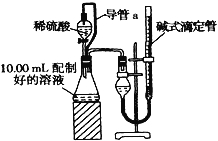
(1)装置中导管a的定量作用是 .
(2)若撤去导管a,使测得气体体积 (“偏大”,“偏小”或“无影响”).
【方案三】:滴定法.量取25.00mL配制好的溶液加入锥形瓶中,滴加2滴酚酞试剂,摇匀,用0.2000molL﹣1的盐酸滴定到终点(已知终点时反应H++CO32﹣═HCO3﹣恰好完全).重复此操作2次,消耗盐酸的体积平均值为20.00mL.
(1)量取25.00mL配制好的溶液,应选择 仪器来完成.
(2)判断滴定终点的依据是 .
(3)此法测得ω(Na2CO3)= %.
【答案】
方案一:(1)D;(2)偏小;
方案二:(1)让锥形瓶中的气体进入分液漏斗上部,保证测量气体体积的准确;(2)偏大;
方案三:(1)碱式滴定管;(2)由红色突变为无色,且30s不恢复;(3)84.8;
【解析】
试题分析:方案一:(1)A.CaCl2溶液只能与碳酸根反应转化为碳酸根沉淀,故A错误;B.MgSO4溶液与HCO3-、CO32-均不反应,故B错误;C.NaCl溶液与HCO3-、CO32-都不反应,故C错误;D.Ba(OH)2溶液与HCO3-、CO32-都发生反应生成碳酸钡沉淀,故D正确;故答案为:D;(2)如果此步中,沉淀未干燥充分就称量,则称量值偏大,由于在质量相等的条件下碳酸氢钠产生的沉淀大于碳酸钠产生的沉淀,所以如果称量值偏大,则碳酸氢钠的质量偏大,则碳酸钠的含量偏小,故答案为:偏小;
方案二:(1)由于碳酸盐与酸反应产生二氧化碳气体,瓶内压强增大,所以装置中导管a的作用是平衡压强、使液体顺利滴下;消除加入稀硫酸引起的体积误差,故答案为:让锥形瓶中的气体进入分液漏斗上部,保证测量气体体积的准确;(2)若撤去导管a会使测得气体体积偏大,故答案为:偏大;
方案三:(1)溶液显碱性,因此应该用碱式滴定管量取,故答案为:碱式滴定管;(2)酚酞的变色范围是8.2~10.0,所以判断滴定终点的依据是由红色突变为无色,且30s不恢复,故答案为:由红色突变为无色,且30s不恢复;(3)反应达到终点时,发生的离子方程式为:H++CO32-=HCO3-,则根据消耗盐酸的体积可知20.00ml可知,消耗碳酸钠的物质的量为:0.2000 mol/L×0.02000L=0.004mol,则原混合物中碳酸钠的物质的量为:0.004mol×![]() =0.04mol,质量为:0.04mol×106g/mol=4.24g,所以碳酸钠质量分数为:
=0.04mol,质量为:0.04mol×106g/mol=4.24g,所以碳酸钠质量分数为:![]() ×100%=84.8%,故答案为:84.8。
×100%=84.8%,故答案为:84.8。

