题目内容
(12分)已知某工业废水中含有大量FeSO4,较多的Cu2+,少量的Na+ 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
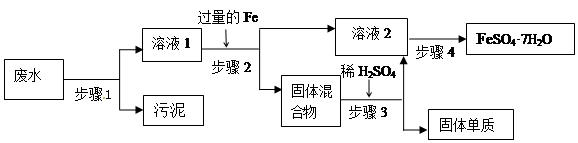
(1)步骤1、步骤2、步骤3的主要操作是 (填“相同”或“不相同”),需用到的玻璃仪器除烧杯外还有 。
(2)步骤2中发生反应的离子方程式为
(3)步骤3中发生反应的化学方程式为
(4)步骤4中涉及的操作是:蒸发浓缩. .过滤.洗涤.烘干。
(5)最后的固体单质是________(填名称)

(1)步骤1、步骤2、步骤3的主要操作是 (填“相同”或“不相同”),需用到的玻璃仪器除烧杯外还有 。
(2)步骤2中发生反应的离子方程式为
(3)步骤3中发生反应的化学方程式为
(4)步骤4中涉及的操作是:蒸发浓缩. .过滤.洗涤.烘干。
(5)最后的固体单质是________(填名称)
(1)相同(2分)、普通漏斗(填漏斗0分)(1分), 玻璃棒(1分)错填0分
(2)Fe2+ + Cu==Cu2+ + 2Fe(2分)
(3)Fe+ H2SO4 ="=" FeSO4 + H2 ↑ (2分无气体符号扣1分)
(4)冷却结晶(或填结晶给1分)(2分) (5)铜(2分填化学式0分)
(2)Fe2+ + Cu==Cu2+ + 2Fe(2分)
(3)Fe+ H2SO4 ="=" FeSO4 + H2 ↑ (2分无气体符号扣1分)
(4)冷却结晶(或填结晶给1分)(2分) (5)铜(2分填化学式0分)
(1)步骤1的目的是除去污泥的,步骤2的目的是除去铁和铜,步骤3的目的是除去铜,所以操作是相同的,都是过滤。过滤需用到的玻璃仪器除烧杯外还有普通漏斗、玻璃棒。
(2)铁的金属性强于铜,所以铁能置换出铜,方程式为Fe2+ + Cu==Cu2+ + 2Fe。
(3)过量的铁能和稀硫酸反应,但铜和稀硫酸不反应,所以方程式为Fe+ H2SO4 ="=" FeSO4 + H2 ↑。
(4)要从溶液中得到硫酸亚铁晶体,应该通过蒸发浓缩、冷却结晶来实现。
(5)铜和稀硫酸不反应,所以最后得到的是铜。
(2)铁的金属性强于铜,所以铁能置换出铜,方程式为Fe2+ + Cu==Cu2+ + 2Fe。
(3)过量的铁能和稀硫酸反应,但铜和稀硫酸不反应,所以方程式为Fe+ H2SO4 ="=" FeSO4 + H2 ↑。
(4)要从溶液中得到硫酸亚铁晶体,应该通过蒸发浓缩、冷却结晶来实现。
(5)铜和稀硫酸不反应,所以最后得到的是铜。

练习册系列答案
相关题目
 、
、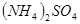 、
、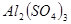 三种溶液的试剂是
三种溶液的试剂是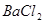 溶液
溶液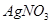 溶液
溶液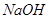 溶液
溶液