题目内容
化学研究性学习小组进行以下实验:

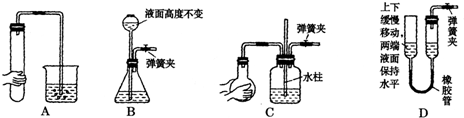
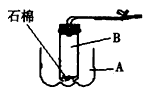
(1)验证醋酸、碳酸和苯酚溶液的酸性强弱的探究实验.利用如图1所示的仪器和药品,设计了一个简单的一次性完成乙酸、碳酸和苯酚溶液酸性强弱验证的实验装置.画出实验装置图并写出验证实验中发生反应的离子方程式(有几个写几个,可以不填满,也可以补充)
①
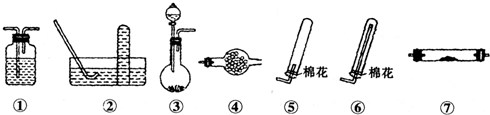
(2)如图2中的实验装置可用于制取乙炔.请填空:
①图2中,A管的作用
②乙炔通入KMnO4酸性溶液中观察到的现象是
③乙炔通入溴的CCl4溶液中观察到的现象是
④为了安全,点燃乙炔前应

(1)验证醋酸、碳酸和苯酚溶液的酸性强弱的探究实验.利用如图1所示的仪器和药品,设计了一个简单的一次性完成乙酸、碳酸和苯酚溶液酸性强弱验证的实验装置.画出实验装置图并写出验证实验中发生反应的离子方程式(有几个写几个,可以不填满,也可以补充)
①
CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O
;②C6H5O-+CO2+H2O→OH+HCO3-
C6H5O-+CO2+H2O→OH+HCO3-
;③无
无
.(2)如图2中的实验装置可用于制取乙炔.请填空:
①图2中,A管的作用
调节水面高度以控制反应的发生和停止
调节水面高度以控制反应的发生和停止
.制取乙炔的化学方程式是CaC2+2H2OCa(OH)2+C2H2↑
CaC2+2H2OCa(OH)2+C2H2↑
.②乙炔通入KMnO4酸性溶液中观察到的现象是
酸性高锰酸钾溶液褪色
酸性高锰酸钾溶液褪色
,乙炔发生了氧化
氧化
反应.③乙炔通入溴的CCl4溶液中观察到的现象是
溴的四氯化碳溶液褪色
溴的四氯化碳溶液褪色
,乙炔发生了加成
加成
反应.④为了安全,点燃乙炔前应
检验乙炔的纯度
检验乙炔的纯度
,乙炔燃烧时的实验现象是火焰明亮并伴有浓烈的黑烟
火焰明亮并伴有浓烈的黑烟
.分析:(1)通过醋酸与碳酸钠反应生成二氧化碳,证明醋酸的酸性大于碳酸;通过二氧化碳与苯酚钠溶液的反应,证明碳酸的酸性大于苯酚酸性;据此画出实验装置图并写出验证实验中发生反应的离子方程式;
(2)①图示装置可通过调节A管的高度,控制反应的发生和停止;
②乙炔能够被酸性高锰酸钾溶液氧化;
③乙炔能够与溴的四氯化碳发生加成反应;
④可燃性气体在点燃前必须检验其纯度;乙炔中含碳的质量分数较大,燃烧时火焰明亮并伴有浓烈的黑烟.
(2)①图示装置可通过调节A管的高度,控制反应的发生和停止;
②乙炔能够被酸性高锰酸钾溶液氧化;
③乙炔能够与溴的四氯化碳发生加成反应;
④可燃性气体在点燃前必须检验其纯度;乙炔中含碳的质量分数较大,燃烧时火焰明亮并伴有浓烈的黑烟.
解答:解:(1)利用醋酸能够与碳酸钠反应生成碳酸,证明乙酸的酸性大于碳酸的酸性,然后把生成的二氧化碳通入苯酚钠溶液中,苯酚钠溶液变浑浊,证明碳酸的酸性强于苯酚的酸性,实验装置图为: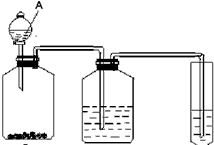 ,涉及的离子方程式为:C6H5O-+CO2+H2O→OH+HCO3-,CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O,
,涉及的离子方程式为:C6H5O-+CO2+H2O→OH+HCO3-,CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O,
故答案为: ;C6H5O-+CO2+H2O→OH+HCO3-;CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;
;C6H5O-+CO2+H2O→OH+HCO3-;CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;
(2)①图示装置可通过调节A管的高度,控制反应的发生和停止:将A管提高,右管中水面上升,与电石接触发生反应;将A管降低,右管中水面下降,水与电石脱离接触,反应停止;实验室通过电石与水的反应制取乙炔:CaC2+2H2OCa(OH)2+C2H2↑,
故答案为:调节水面高度以控制反应的发生和停止;CaC2+2H2OCa(OH)2+C2H2↑;
②乙炔含有不饱和键,能够与高锰酸钾溶液发生了氧化还原反应,使高锰酸钾溶液褪色,
故答案为:酸性高锰酸钾溶液褪色;氧化;
③乙炔含有碳碳双键,能使溴的四氯化碳溶液褪色,发生了加成反应,
故答案为:溴的四氯化碳溶液褪色;加成;
④乙炔等可燃性气体在点燃前必须检验其纯度,以免发生爆炸;因乙炔中含碳的质量分数较大,在燃烧时火焰明亮并伴有浓烈的黑烟,
故答案为:检验乙炔的纯度;火焰明亮并伴有浓烈的黑烟.
 ,涉及的离子方程式为:C6H5O-+CO2+H2O→OH+HCO3-,CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O,
,涉及的离子方程式为:C6H5O-+CO2+H2O→OH+HCO3-,CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O,故答案为:
 ;C6H5O-+CO2+H2O→OH+HCO3-;CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;
;C6H5O-+CO2+H2O→OH+HCO3-;CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O;(2)①图示装置可通过调节A管的高度,控制反应的发生和停止:将A管提高,右管中水面上升,与电石接触发生反应;将A管降低,右管中水面下降,水与电石脱离接触,反应停止;实验室通过电石与水的反应制取乙炔:CaC2+2H2OCa(OH)2+C2H2↑,
故答案为:调节水面高度以控制反应的发生和停止;CaC2+2H2OCa(OH)2+C2H2↑;
②乙炔含有不饱和键,能够与高锰酸钾溶液发生了氧化还原反应,使高锰酸钾溶液褪色,
故答案为:酸性高锰酸钾溶液褪色;氧化;
③乙炔含有碳碳双键,能使溴的四氯化碳溶液褪色,发生了加成反应,
故答案为:溴的四氯化碳溶液褪色;加成;
④乙炔等可燃性气体在点燃前必须检验其纯度,以免发生爆炸;因乙炔中含碳的质量分数较大,在燃烧时火焰明亮并伴有浓烈的黑烟,
故答案为:检验乙炔的纯度;火焰明亮并伴有浓烈的黑烟.
点评:本题考查了酸性强弱比较、乙炔的制备、性质检验以及方程式的书写,题目难度中等,该题是高考中的常见题型,属于中等难度的试题;试题基础性强,在注重对学生基础知识训练和检验的同时,侧重对学生实验答题能力的培养和方法与技巧的指导和训练,有利于提高学生的实验设计能力和应试能力,提升学生的学科素养.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
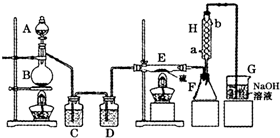
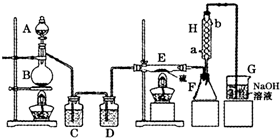
 某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,绘制了如下装置简图.
某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,绘制了如下装置简图.