题目内容
(1)把NaHCO3和Na2CO3·10H2O混合物6.56g溶于水制成100ml溶液,测得溶液中c(Na+)=0.5mol/L。
向该溶液中加入盐酸至不再产生气体为止,将溶液蒸干后,所得固体质量为___________。
(2)将24.0g氢氧化钠固体放入水中,要使100个水分子中就含有一个Na+离子,所需水的质量为_________________。
(3)现有HNO3和NaNO3的混合溶液200mL,其中 HNO3和NaNO3的物质的量浓度均为1mol/L.若要使 HNO3和NaNO3 的物质的量浓度分别为2mol/L 和0.2mol/L,则须加入63%的浓硝酸(密度为1.2g/cm3)___________mL,再加入蒸馏水稀释至_______毫升才能实现。
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、___________、___________。
(2)量取反应物时, 取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是___________。
取50 mL 0.50 mol·L-1的盐酸,还需加入的试剂是___________。
A.50 mL 0.50 mol·L-1 NaOH溶液 B.50 mL 0.55 mol·L-1 NaOH溶液 C.1.0 g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得中和热ΔH的数值 (填偏大、偏小、无影响)。
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如下表所示。
反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/ kJ·mol-1 |
A.1.0 mol/L HCl溶液50 mL、1.1 mol/L NaOH溶液50 mL | 13.0 | 19.8 ℃ | ΔH1 |
B.1.0 mol/L HCl溶液50 mL、1.1 mol/L NH3·H2O溶液50 mL | 13.0 | 19.3 ℃ | ΔH2 |
① 设充分反应后溶液的比热容c=4.18 J/(g·℃),忽略实验仪器的比热容及溶液体积的变化,则ΔH1= ;ΔH2= 。(已知溶液密度 均为1 g/cm3)
② ΔH1 ≠ ΔH2原因是 。
从H、O、S、K四种元素中选择适当的元素,组成与表中第一行物质类别相同的物质,将其化学式天子表中相应空格内
示例 | HN03 | NaOH | Na2CO3 | CO2 |
化学式 |


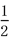 O2(g)=CO(g);△H=-393.5kJ/mol
O2(g)=CO(g);△H=-393.5kJ/mol