��Ŀ����
(9��)
����Ч�ļ���ȼ�ϵ�ز��ò�Ϊ�缫���ϣ����缫�Ϸֱ�ͨ��CH4��O2 �������ΪKOH��Һ��ij�о�С�齫��������ȼ�ϵ�ش�������Ϊ��Դ�����б�����������Һ���ʵ�飬��ͼ��ʾ��
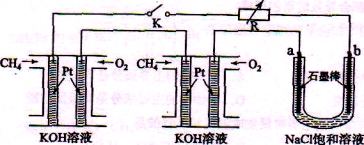
�ش��������⣺
(1)����ȼ�ϵ�������������ĵ缫��Ӧ�ֱ�Ϊ �� ��
(2)�պ�K���غ�a��b�缫�Ͼ����������������b�缫�ϵõ����� ������Ȼ�����Һ���ܷ�Ӧ����ʽΪ ��
(3)��ÿ����ؼ���ͨ����Ϊ1 L(��״��)���ҷ�Ӧ��ȫ����������ͨ�����صĵ���Ϊ
�������ڳ���F=9.65��l04C.mol-1����ʽ����)������ܲ������������Ϊ L(��״��)��
����1��O2+2H2O +4e��=4OH����CH4+10OH--8e��=CO32-+ 7H2O����2��H2��2NaCl+2H2O 2NaOH+ H2��+ Cl2������3����1L/22.4L.mol-1����8��9.65�� 104C.mol-1 =3.45��104C��4��
2NaOH+ H2��+ Cl2������3����1L/22.4L.mol-1����8��9.65�� 104C.mol-1 =3.45��104C��4��
������������1��ȼ�ϵ�ص��ܷ�Ӧ����ȼ��ȼ�յķ�Ӧ����CH4+2O2+2OH- = CO32-+ 3H2O������������ӦʽΪ��O2+ 2H2O +4e��= 4OH�����������ܷ�Ӧʽ��������Ӧʽ�ɵ�������Ӧʽ��CH4+10OH--8e��=CO32-+ 7H2O����2����ͼ�����ؿɿ���1��2������������ȼ�ϵ�أ�ͨ��������һ�����������ʴ˵���������������b�缫Ϊ����������������Ϊ�����������ܷ�ӦʽΪ��2NaCl+2H2O 2NaOH+ H2��+ Cl2������3�����ݣ�1���еĸ�����Ӧʽ����֪ͨ��1mol����ʱʧ����8mol��������Ϊ8��96500C������ͼ�е���������Ǵ������ʿ�֪��·��ת�Ƶĵ�����һ��ȼ�ϵ��ʱ��ͬ����ϼ����������1LΪ1/22.4mol�������Ϊ����1L/22.4L.mol-1����8��9.65�� 104C.mol-1 =3.45��104C�����ʱ�õ�����Ϊ4L��
2NaOH+ H2��+ Cl2������3�����ݣ�1���еĸ�����Ӧʽ����֪ͨ��1mol����ʱʧ����8mol��������Ϊ8��96500C������ͼ�е���������Ǵ������ʿ�֪��·��ת�Ƶĵ�����һ��ȼ�ϵ��ʱ��ͬ����ϼ����������1LΪ1/22.4mol�������Ϊ����1L/22.4L.mol-1����8��9.65�� 104C.mol-1 =3.45��104C�����ʱ�õ�����Ϊ4L��
�����㶨λ��������ȼ�ϵ�ص�ʹ��Ϊ���壬������ԭ��صĵ缫��Ӧʽ��д���缫���жϺ͵��֪ʶ��








