题目内容
化工生产中用烷烃和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇或合成氨,对甲烷而言,有如下两个主要反应:
①CH4(g)+1/2O2(g) CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
②CH4(g)+H2O(g) CO(g)+3H2(g) ΔH2="+216" kJ·mol-1
CO(g)+3H2(g) ΔH2="+216" kJ·mol-1
由反应①②推出总反应热为零的总反应方程式③,并求进料气中空气(O2的体积分数为21%)与水蒸气的体积比。
①CH4(g)+1/2O2(g)
 CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
CO(g)+2H2(g) ΔH1=-36 kJ·mol-1②CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH2="+216" kJ·mol-1
CO(g)+3H2(g) ΔH2="+216" kJ·mol-1由反应①②推出总反应热为零的总反应方程式③,并求进料气中空气(O2的体积分数为21%)与水蒸气的体积比。
100∶7
从所给的热化学方程式可看出:216/36=6,将①×6得出式子与②相加:
6CH4+3O2 6CO+12H2
6CO+12H2
+)CH4+H2O CO+3H2
CO+3H2
7CH4+3O2+H2O 7CO+15H2。
7CO+15H2。
所以总反应式③为
7CH4(g)+3O2(g)+H2O(g) 7CO(g)+15H2(g) ΔH=0
7CO(g)+15H2(g) ΔH=0
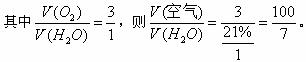
6CH4+3O2
 6CO+12H2
6CO+12H2+)CH4+H2O
 CO+3H2
CO+3H27CH4+3O2+H2O
 7CO+15H2。
7CO+15H2。所以总反应式③为
7CH4(g)+3O2(g)+H2O(g)
 7CO(g)+15H2(g) ΔH=0
7CO(g)+15H2(g) ΔH=0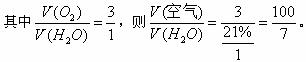

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
