题目内容
【题目】在一定温度下的定容容器中,当下列各量不再发生变化时,表明反应A(g)+2B(g) ![]() C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体的总物质的量⑤混合气体的平均相对分子质量⑥v(C)与v(D)的比值⑦混合气体的总质量⑧混合气体的总体积⑨C、D的分子数之比为1∶1
A.①②③④⑤⑥⑦⑧ B.①③④⑤⑧⑨ C.①②③④⑤⑦ D.①③④⑤
【答案】D
【解析】
试题分析:①、由A(g)+2B(g) ![]() C(g)+D(g)可知,1+2=3>1+1=2,即正反应是气体物质的量减小的方向,同温同容下阿伏加德罗定律的推论
C(g)+D(g)可知,1+2=3>1+1=2,即正反应是气体物质的量减小的方向,同温同容下阿伏加德罗定律的推论![]() 可知,混合气体的压强逐渐减小(或是一个变量),当变量不再发生变化时,说明已达平衡,①正确;②、由
可知,混合气体的压强逐渐减小(或是一个变量),当变量不再发生变化时,说明已达平衡,①正确;②、由![]() 、质量守恒定律和题意可知,混合气体的质量不变,容器的容积也不变,因此混合气体的密度始终不变(或是一个不变量),不变量不再改变不能说明已达平衡,②错误;③、随着反应的进行,反应物(或生成物)的物质的量浓度逐渐减小(或增大)(或是一个变量),变量不再改变能说明已达平衡,③正确;④、由于正反应是气体物质的量减小的方向,随着反应的进行,混合气体的总物质的量逐渐减小(或是一个变量),变量不再改变能说明已达平衡,④正确;⑤、由
、质量守恒定律和题意可知,混合气体的质量不变,容器的容积也不变,因此混合气体的密度始终不变(或是一个不变量),不变量不再改变不能说明已达平衡,②错误;③、随着反应的进行,反应物(或生成物)的物质的量浓度逐渐减小(或增大)(或是一个变量),变量不再改变能说明已达平衡,③正确;④、由于正反应是气体物质的量减小的方向,随着反应的进行,混合气体的总物质的量逐渐减小(或是一个变量),变量不再改变能说明已达平衡,④正确;⑤、由![]() 、质量守恒定律、正反应是气体物质的量减小的方向可知,混合气体的平均相对分子质量逐渐减小(或是一个变量),变量不再改变能说明已达平衡,⑤正确;⑥、由于A(g)+2B(g)
、质量守恒定律、正反应是气体物质的量减小的方向可知,混合气体的平均相对分子质量逐渐减小(或是一个变量),变量不再改变能说明已达平衡,⑤正确;⑥、由于A(g)+2B(g) ![]() C(g)+D(g)中任意两种物质表示的平均反应速率之比等于系数之比,则v(C)∶v(D)始终等于1∶1(或是一个不变量),不变量不再改变不能说明已达平衡,⑥错误;⑦、由于A、B、C、D均是气体,由质量守恒定律可知,密闭容器中混合气体的总质量始终不变(或是一个不变量),不变量不再改变不能说明已达平衡,⑦错误;⑧、由题意可知,容器的容积保持一定,则混合气体的总体积保持恒定(或是一个不变量),不变量不再改变不能说明已达平衡,⑧错误;⑨、C、D的起始物质的量都是0,变化的物质的量相等(等于系数之比),则C、D的分子数之比始终为1∶1二者平衡时的物质的量相等(或是一个不变量),不变量不再改变不能说明已达平衡,⑨错误;答案选D。
C(g)+D(g)中任意两种物质表示的平均反应速率之比等于系数之比,则v(C)∶v(D)始终等于1∶1(或是一个不变量),不变量不再改变不能说明已达平衡,⑥错误;⑦、由于A、B、C、D均是气体,由质量守恒定律可知,密闭容器中混合气体的总质量始终不变(或是一个不变量),不变量不再改变不能说明已达平衡,⑦错误;⑧、由题意可知,容器的容积保持一定,则混合气体的总体积保持恒定(或是一个不变量),不变量不再改变不能说明已达平衡,⑧错误;⑨、C、D的起始物质的量都是0,变化的物质的量相等(等于系数之比),则C、D的分子数之比始终为1∶1二者平衡时的物质的量相等(或是一个不变量),不变量不再改变不能说明已达平衡,⑨错误;答案选D。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案【题目】下列图象中,纵坐标为沉淀物的量,横坐标为溶液中加入反应物的物质的量,试按题意将图象中相应的数字序号填入表中的顺序为
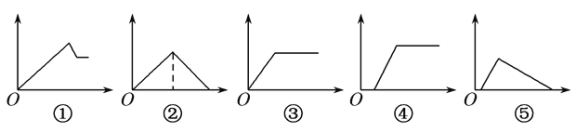
溶液 | 加入物质 | 相应序号 |
(1)氯化铝溶液 | 加入过量氨水 | |
(2)饱和澄清石灰水 | 通入过量CO2气体 | |
(3)含少量NaOH的偏铝酸钠溶液 | 通入过量CO2气体 | |
(4)含少量NaOH的偏铝酸钠溶液 | 逐滴加入稀盐酸 | |
(5)MgCl2、AlCl3的混合溶液 | 逐滴加入NaOH溶液至过量 |
A. ①③②④⑤ B. ③⑤④②①
C. ①②③④⑤ D. ③②④⑤①


