题目内容
设NA为阿佛加德罗常数,下列说法正确的是
- A.12克金刚石中含共价键数目为4NA
- B.78克Na2O2与过量的CO2充分反应,转移电子数为NA
- C.标准状况下22.4LHCl气体溶于水,其溶液中H+数约为NA
- D.1mol羟基与1molNH4+所含电子数均为10NA
BC
分析:A、一个碳原子能形成2个共价键,根据N=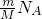 结合每个碳原子具有的共价键个数计算.
结合每个碳原子具有的共价键个数计算.
B、根据过氧化钠和转移电子之间的关系式计算.
C、根据N= 计算含有的氯化氢分子数,然后结合氯化氢的分子构成计算氢离子个数.
计算含有的氯化氢分子数,然后结合氯化氢的分子构成计算氢离子个数.
D、根据N=nNA结合每个微粒中含有的电子数计算电子个数.
解答:A、一个碳原子能含有2个共价键,12g金刚石的物质的量是1mol,所以12g金刚石中含共价键数目为2NA,故A错误.
B、2Na2O2+2CO2=2Na2CO3+O2转移电子
156g 2NA
78g NA
所以78gNa2O2与过量的CO2充分反应,转移电子数为NA,故B正确.
C、标况下,22.4LHCl气体的物质的量为1mol,一个氯化氢分子中含有一个氢原子,所以氯化氢溶于水,其溶液中H+数约为NA,故C正确.
D、一个羟基中含有9个电子,一个NH4+含有10电子,所以1mol羟基中含有电子数为9NA,1molNH4+所含电子数为10NA,故D错误.
故选BC.
点评:本题考查了阿伏伽德罗常数的有关计算,难度较大,难点是判断金刚石中一个碳原子含有的共价键个数.
分析:A、一个碳原子能形成2个共价键,根据N=
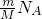 结合每个碳原子具有的共价键个数计算.
结合每个碳原子具有的共价键个数计算.B、根据过氧化钠和转移电子之间的关系式计算.
C、根据N=
 计算含有的氯化氢分子数,然后结合氯化氢的分子构成计算氢离子个数.
计算含有的氯化氢分子数,然后结合氯化氢的分子构成计算氢离子个数.D、根据N=nNA结合每个微粒中含有的电子数计算电子个数.
解答:A、一个碳原子能含有2个共价键,12g金刚石的物质的量是1mol,所以12g金刚石中含共价键数目为2NA,故A错误.
B、2Na2O2+2CO2=2Na2CO3+O2转移电子
156g 2NA
78g NA
所以78gNa2O2与过量的CO2充分反应,转移电子数为NA,故B正确.
C、标况下,22.4LHCl气体的物质的量为1mol,一个氯化氢分子中含有一个氢原子,所以氯化氢溶于水,其溶液中H+数约为NA,故C正确.
D、一个羟基中含有9个电子,一个NH4+含有10电子,所以1mol羟基中含有电子数为9NA,1molNH4+所含电子数为10NA,故D错误.
故选BC.
点评:本题考查了阿伏伽德罗常数的有关计算,难度较大,难点是判断金刚石中一个碳原子含有的共价键个数.

练习册系列答案
相关题目
设NA、表示阿佛加德罗常数值,下列说法正确的是
| A.1000mL0.1mol·L-1的Al2(SO4)3溶液中,含Al3+ 0.1NA |
| B.在标准状况下,11.2L氖气中含有NA个氖原子 |
| C.7.8gNa2O2与足量CO2反应,转移电子数为0.1NA |
| D.62 g Na2O溶于水后所得溶液中含有O2-离子数为NA |