题目内容
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为Va、Vb,则两者的关系正确的是( )
分析:醋酸为弱电解质,浓度越大,电离程度越小,pH为2和3的CH3COOH溶液,后者电离程度大,根据含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,二者物质的量相等判断.
解答:解:含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,则有二者物质的量相等,因为所中和的氢氧化钠的物质的量是一定的,而醋酸是弱酸,醋酸为弱电解质,浓度越大,电离程度越小,pH为2和3的CH3COOH溶液,后者电离程度大,pH为2的CH3COOH的浓度大于pH为3的CH3COOH溶液的浓度的10倍,
设pH为2的醋酸浓度为x,PH=3的醋酸浓度为y,则有Va×x=Vb×y,
则
=
<
,即Vb>10Va,
故选D.
设pH为2的醋酸浓度为x,PH=3的醋酸浓度为y,则有Va×x=Vb×y,
则
| Va |
| Vb |
| y |
| x |
| 1 |
| 10 |
故选D.
点评:本题考查酸碱混合的计算,题目难度较大,本题注意浓度不同的醋酸,电离程度不同,浓度越大,电离程度越小.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列图示与对应叙述相符合的是( )
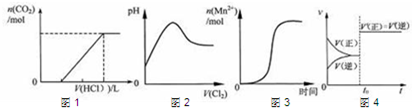

| A、图1表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol?L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 | B、图2表示Cl2通入SO2溶液中pH的变化 | C、图3表示10 mL 0.01 mol?L-1KMnO4 酸性溶液与过量的0.1 mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用) | D、图4表示已达平衡的某可逆反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |