题目内容
相同物质的量的铝箔分别与足量的稀盐酸、浓氢氧化钠溶液反应,待完全反应后,产生的气体的体积比为( )
| A、2:3 | B、3:1 |
| C、1:1 | D、1:2 |
考点:铝的化学性质
专题:计算题,元素及其化合物
分析:铝与盐酸、氢氧化钠分别发生:2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑,结合反应的方程式计算.因酸碱都是足量的,则铝完全反应,铝的物质的量相等,则生成的氢气的量相等.
解答:
解:由2Al+2NaOH+2H2O═2NaAlO2+3H2↑、2Al+6HCl═2AlCl3+3H2↑可知,
2molAl分别与足量酸、碱反应都生成3molH2,
则两份物质的量的铝粉分别与足量酸、碱反应生成等量的氢气,
氢气的物质的量之比等于其体积之比,则相同状态下产生的气体体积之比是1:1,
故选C.
2molAl分别与足量酸、碱反应都生成3molH2,
则两份物质的量的铝粉分别与足量酸、碱反应生成等量的氢气,
氢气的物质的量之比等于其体积之比,则相同状态下产生的气体体积之比是1:1,
故选C.
点评:本题考查学生利用酸碱与铝的反应进行计算,关键是清楚发生的化学反应及金属Al完全反应是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、蛋白质和糖类的水解都是高分子生成小分子的过程 |
| B、甲苯分子中所有原子均处在同一个平面上 |
| C、溴水与乙烯发生加聚反应而褪色 |
| D、天然气和液化石油气的主要成分都是烃 |
下各各组物质中,前者是纯净物,后者是混合物的是( )
| A、水煤气、汽油 |
| B、盐酸、碳酸钙 |
| C、硫酸铜晶体、氢氧化铁胶体 |
| D、铁锈、小苏打 |
下列叙述正确的是( )
| A、氮在自然界的循环过程中存在形式既有游离态又有化合态,但化合态中没有铵盐 |
| B、按照分散质和分散剂所处状态的不同可以把分散系分为9种类型 |
| C、能使品红溶液褪色的气体一定是SO2 |
| D、某无色溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液-定含有SO42- |
下列关于苯的说法中,不正确的是( )
| A、分子中含有三个C-C键和三个C=C键 |
| B、在空气中燃烧时产生较多的黑烟 |
| C、分子中C、H元素的质量为12:1 |
| D、在一定条件下可与氢气发生加成反应 |
某有机样品3.1g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g,经过滤得到10g沉淀.该有机样品可能是( )
| A、乙二醇 | B、乙醇 |
| C、乙醛 | D、甲醇和乙醇的混合物 |
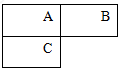 A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是( )
A、B、C三种短周期元素在周期表中的位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和等于C的质子数,则下列说法正确的组合是( )①B、C形成的单质均存在同素异形体
②X的种类比Y多
③常温下,B的氢化物不能电离出H+
④C的最高价氧化物对应的水化物是强酸.
| A、①②③④ | B、②④ |
| C、①② | D、①③ |
下列说法正确的是( )
| A、铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应 |
| B、硅在电子工业中是最重要的半导体材料,广泛用于制作光导纤维 |
| C、二氧化硫是一种有毒气体,所以不能用于杀菌消毒 |
| D、氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |