题目内容
(2009?松江区二模)常温下,现有a mol/L NaX溶液和b mol/L NaY溶液,关于它们的说法错误的是( )
分析:A、根据水解规律:越弱越水解以及酸性越弱,弱酸阴离子水解越强来回答;
B、c(X-)=c(Y-)+c(HY),X-没有水解,因此为强酸;
C、根据水解规律:越弱越水解以及酸性越弱,弱酸阴离子水解越强来回答;
D、根据溶液混合以前存在的物料守恒来判断.
B、c(X-)=c(Y-)+c(HY),X-没有水解,因此为强酸;
C、根据水解规律:越弱越水解以及酸性越弱,弱酸阴离子水解越强来回答;
D、根据溶液混合以前存在的物料守恒来判断.
解答:解:只有弱酸的酸根才发生水解的,酸性越弱,水解越强.
A、两种溶液浓度相同,pH(NaX)>pH(NaY),说明NaX的碱性更强,对应的X-的水解程度更强,因此酸性HX<HY,故A错误;
B、a=b而且c(X-)=c(Y-)+c(HY),因此可以看出X-没有水解,因此为强酸,故酸性HX>HY,故B正确;
C、a>b并且c(X-)=c(Y-),可以得知X-水解的部分大于Y-水解的部分,所以c(HX)>c(HY),并且相同浓度时,酸性HX<HY,故C正确;
D、两种溶液混合以前,a=c(X-)+c(HX),b=c(Y-)+c(HY),若等体积混合,则混合后的体积是混合前的两倍,所以c(X-)+c(Y-)+c(HX)+c(HY)=
(a+b),又因为c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,所以得到a+b=0.2mol/L,但并不能得到a=b=0.1mol/L,故D错误.
故选AD.
A、两种溶液浓度相同,pH(NaX)>pH(NaY),说明NaX的碱性更强,对应的X-的水解程度更强,因此酸性HX<HY,故A错误;
B、a=b而且c(X-)=c(Y-)+c(HY),因此可以看出X-没有水解,因此为强酸,故酸性HX>HY,故B正确;
C、a>b并且c(X-)=c(Y-),可以得知X-水解的部分大于Y-水解的部分,所以c(HX)>c(HY),并且相同浓度时,酸性HX<HY,故C正确;
D、两种溶液混合以前,a=c(X-)+c(HX),b=c(Y-)+c(HY),若等体积混合,则混合后的体积是混合前的两倍,所以c(X-)+c(Y-)+c(HX)+c(HY)=
| 1 |
| 2 |
故选AD.
点评:本题考查学生溶液中的离子浓度之间的关系知识,考查学生分析和解决问题的能力,难度较大.

练习册系列答案
相关题目
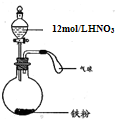 (2009?松江区二模)如图所示,向一定量的铁粉中加入一定体积12mol/L的硝酸,加热充分反应后,下列微粒在体系中可能大量存在的是( )
(2009?松江区二模)如图所示,向一定量的铁粉中加入一定体积12mol/L的硝酸,加热充分反应后,下列微粒在体系中可能大量存在的是( )