题目内容
某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子。以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4·7H2O)和汞的方案。
【药品】NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉
【实验方案】
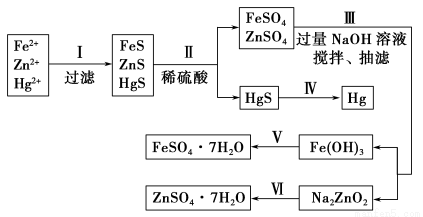
【问题探究】
(1)步骤Ⅱ所发生反应的离子方程式为 。
(2)步骤Ⅲ中抽滤的目的是 ,该步骤产生Fe(OH)3的反应的离子方程式为 。
(3)步骤Ⅵ中得到硫酸锌溶液的离子方程式为 。
(4)欲实现步骤Ⅴ,需加入的试剂有 、 ,所涉及的主要操作依次为 。
(5)步骤Ⅳ常用的方法是 ,该步骤是否对环境有影响? (填“是”或“否”),如有影响,请你设计一个绿色环保方案来实现步骤Ⅳ的反应: 。
(6)该研究小组的同学在强碱溶液中,用次氯酸钠与Fe(OH)3反应获得了高效净水剂Na2FeO4,该反应的离子方程式为 。
(1)FeS+2H+=Fe2++H2S↑、ZnS+2H+=Zn2++H2S↑
(2)加快过滤 4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓(分步书写也可)
(3)ZnO22-+4H+=Zn2++2H2O
(4)稀硫酸 铁粉(过量) 过滤、浓缩结晶
(5)加热 是 在密闭容器中加热HgS
(6)3ClO-+2Fe(OH)3+4OH-=2FeO42-+3Cl-+5H2O
【解析】(1)步骤Ⅱ中只有FeS、ZnS固体溶解在稀硫酸中生成FeSO4、ZnSO4,反应的离子方程式为FeS+2H+=Fe2++H2S↑、ZnS+2H+=Zn2++H2S↑。
(2)抽滤时产生负压,能加快过滤。向FeSO4和ZnSO4的混合溶液中加入过量NaOH溶液时,Fe2+与OH-反应生成Fe(OH)2,Fe(OH)2迅速被空气中的O2氧化为Fe(OH)3,其反应的离子方程式为4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓。
(3)根据框图转化关系,不难发现Zn(OH)2的性质类似于Al(OH)3的,Na2ZnO2的性质类似于NaAlO2的,所以向Na2ZnO2的溶液中加入过量H2SO4生成ZnSO4溶液,其反应的离子方程式为ZnO22-+4H+=Zn2++2H2O。
(4)Fe(OH)3首先与稀H2SO4反应生成Fe2(SO4)3,Fe2(SO4)3再与过量的Fe粉反应得到FeSO4。经过滤除去Fe粉,将滤液经过浓缩结晶可得FeSO4·7H2O。
(5)HgS在空气中加热可得Hg、SO2,由于Hg蒸气和SO2都会对环境造成污染,在密闭容器中加热HgS可有效防止Hg蒸气和SO2释放到大气中,从而保护了环境。
(6)反应物有ClO-、Fe(OH)3、OH-,生成物有Cl-、FeO42-、H2O,则有ClO-+Fe(OH)3+OH-―→FeO42-+Cl-+H2O,再将该离子方程式配平即可。

已知一定温度下,有下列难溶电解质的溶解平衡数据:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp/25 ℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
则对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是 ( )。
A.向该混合溶液中加过量铁粉,能观察到红色固体析出
B.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
C.该混合溶液中c(SO42-)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
D.向该混合溶液中加入适量氯水,并调节pH至3~4后过滤,能得到纯净的CuSO4溶液