题目内容
能在水溶液中大量共存的离子组是
| A.H+ Fe3+ ClO-Cl- |
| B.H+ NH4+Fe2+ NO3- |
| C.Ag+ K+ Cl-SO42- |
| D.K+ AlO2-Cl- OH- |
D
解析试题分析:A、H+与ClO?反应生成弱酸HClO,故不能共存;B、H+、NO3?氧化Fe2+,故不能共存;C、Ag+与Cl?反应生成AgCl沉淀,故不能共存;D、离子间互相不反应,故能大量共存。
考点:本题考查离子共存

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
某溶液中含有AlO2-、SO32-、SO42-、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是
| A.SO32- | B.Na+ | C.AlO2- | D.SO42- |
常温下,在下列各组溶液中,加水稀释时c(OH-) / c(H+)值明显增大,且能大量共存的离子组是( )
① K+、Al3+、NO3-、AlO2- ② K+、Fe3+、I-、SO42-
③ Ba2+、I-、NO3-、Na+ ④ Na+、Ca2+、Al3+、 Cl-
| A.①② | B.①③ | C.②④ | D.②③ |
下列离子方程式书写正确的是
| A.澄清石灰水与少量小苏打溶液混合:Ca2+ +2OH- +2HCO3- = CaCO3↓+ CO32- + 2H2O |
| B.氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = Al(OH)4-↓+ 4NH4+ |
| C.少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O=2C6H5OH+ CO32- |
| D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全:Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O |
下列各组离子—定能大量共存的是( )。
| A.在含有大量AlO2-的溶液中:NH4+、Na+、Cl-、H+ |
| B.在pH=12的溶液中:NH4+、Na+、(SO3)2-、Cl- |
| C.在强碱溶液中:Na+、K+、CO32-、NO3- |
D.在 c(H+)=0.1mol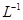 的溶液中:K+、I-、Cl-、NO3- 的溶液中:K+、I-、Cl-、NO3- |
下列物质属于非电解质的是
| A.金属钠 | B.CaCl2 | C.H2SO4 | D.SO2 |
向Na2CO3、NaHCO,混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是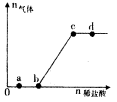
| A.a点对应的溶液中:Na+、OH—、SO2—4、NO—3 |
| B.b点对应的溶液中:Al3+、Fe3+、MnO—4、Cl— |
| C.c点对应的溶液中:Na+.Ca2+.NO—3、Cl— |
| D.d点对应的溶液中:F—、NO—3、Fe2+、Ag+ |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.遇Fe(CN)63-显蓝色的溶液:Ca2+、 Cl-、ClO-、Fe3+ |
| B.水电离出c(OH-)>10-5mol/L: Mg2+、 Cl-、NO3-、Na+; |
| C.遇石蕊变红的溶液:Na+、 NH4+、NO3-、K+ |
| D.与铝反应产生大量氢气的溶液:Ba2+、 HCO3- 、l- 、Fe2+ |
下列离子方程式中,正确的是
| A.用惰性电极电解MgCl2溶液:2Cl—+H2O通电 2OH—+Cl2↑+H2↑ |
B.碳酸钠溶液显碱性:CO32—+H2O HCO3—+OH— HCO3—+OH— |
C.氯气通入冷水中:Cl2 +H2O  Cl- +ClO- +2H+ Cl- +ClO- +2H+ |
| D.碳酸镁悬浊液中加醋酸:CO32-+2CH3COOH= 2CH3COO-+CO2↑+H2O |