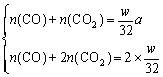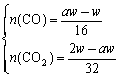题目内容
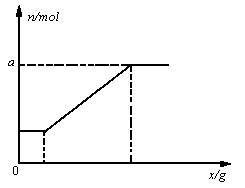
将碳粉与wg氧气置于密闭容器中,经高温充分反应后,恢复至初始温度,测得反应前后压强分别为p0,p,并且p=np0,加入的碳粉质量xg与n的变化关系如下图所示。(已知同温同容下,气体反应前后物质的量之比等于反应前后压强之比)
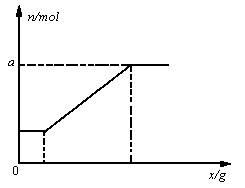
(1)n的最小值是________,此时x的取值范围是____________________________________。
(2)n的最大值是________,此时x的取值范围是____________________________________。
(3)若实验结果测得n值为a,求容器内气体的体积之比。
答案:
解析:
解析:
解:碳与氧气反应,根据两者相对量的不同,可能发生两种反应: 反应:C+O2 2C+O2 (1)若反应按①式进行,反应前后气体的物质的量不变,所以压强不变,p最小,n=1。要使反应按①式进行,需满足n(C)£n( (2)当n(C)³2n(O2)时,反应肯定按②式进行,反应后的气体的物质的量是原来的2倍,此时p最大,则x³ (3)若
Þ 故n(CO)/n( 答案:(1)1 xÎ(0, (2)2 xÎ[ (3)(2a-2)/(2-a)
|

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目