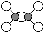
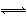
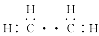题目内容
标准状况下1.68 L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水中,得到的白色沉淀质量为15.0 g;若用足量碱石灰吸收燃烧产物,质量增加9.3 g。
(1)燃烧产物中生成水的质量是______________________________。
(2)若原气体是单一气体,则它的分子式是___________________________。
(3)若原气体是两种等物质的量的气体的混合物,其中只有一种是烃,请写出它们的分子式(只要求写出一组)___________________________。
(1)2.7 g (2)C2H4 (3)C3H8与CO(或C4H6与H2、C3H6与CH2O等)
【解析】(1)白色沉淀为CaCO3,对应的CO2为0.15 mol,即6.6 g,碱石灰吸收的是H2O和CO2,因此H2O的质量为2.7 g。(2)1.68 L无色气体的物质的量为0.075 mol,得出气体分子中碳、氢原子数分别为2、4,如果是单一气体,分子式为C2H4。(3)由于混合物中两气体物质的量相等,所以只要两气体的碳、氢原子数的平均值分别为2、4就能满足条件。

)实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到55~60 ℃反应,已知苯与硝基苯的基本物理性质如下表所示:
| 熔点 | 沸点 | 状态 |
苯 | 5.51 ℃ | 80.1 ℃ | 液体 |
硝基苯 | 5.7 ℃ | 210.9 ℃ | 液体 |
(1)要配制浓硫酸和浓硝酸的混合酸的注意事项是_________。
(2)分离硝基苯和水的混合物的方法是________;分离硝基苯和苯的方法是__________________________。
(3)某同学用如图装置制取硝基苯:
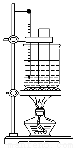
①用水浴加热的优点是_____________________;
②指出该装置的两处缺陷___________________;___________。