题目内容
【题目】下面这个实验为“套管实验”,实验装置如下图,请观察实验装置。分析实验原理,并回答下列问题:
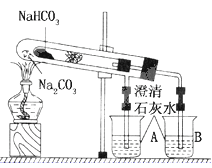
(1)整个实验过程中,能观察到①烧杯A中的现象:②烧杯B中的现象______________;
(2)实验结束时的操作是______________
(3)写出实验过程中发生反应的化学方程式______________;
(4)该实验可证明稳定性:NaHCO3 Na2CO3(填大于,小于或等于),证明稳定性比较时,能否将NaHCO3、Na2CO3的位置互换 (填能或不能)。
【答案】(1)①有气泡冒出;
②有气泡产生,澄清石灰水变浑浊
(2)先将导气管从A、B的烧杯中取出,再停止加热
(3)2NaHCO3![]() Na2CO3+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
Na2CO3+H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
(4)小于;不能
【解析】
试题分析:(1)①实验开始时,大试管中的气体受热膨胀,烧杯A的导气管中会有气泡冒出。
②碳酸氢钠加热分解生成二氧化碳气体,二氧化碳与澄清石灰水反应生成碳酸钙沉淀,所以烧杯B中导气管中有气泡产生,澄清石灰水变浑浊。
(2)实验结束时,在操作上要特别注意:先将导气管从A、B烧杯中取出,再停止加热,以防倒吸。
(3)实验过程中发生反应的化学方程式有:小试管中碳酸氢钠受热分解生成碳酸钠、二氧化碳气体和水:2NaHCO3![]() Na2CO3+CO2↑+H2O;二氧化碳与澄清石灰水反应生成碳酸钙沉淀,所以烧杯B中发生反应:CO2+Ca(OH)2=CaCO3↓+H2O。
Na2CO3+CO2↑+H2O;二氧化碳与澄清石灰水反应生成碳酸钙沉淀,所以烧杯B中发生反应:CO2+Ca(OH)2=CaCO3↓+H2O。
(4)碳酸氢钠在小试管,碳酸钠在大试管,大试管直接加热,温度较高。依据温度较高的不分解,而加热温度较低的物质分解,可判断稳定Na2CO3小于NaHCO3,NaHCO3分解有CO2和H2O产生。且Na2CO3与NaHCO3的位置不能不换。

