题目内容
据报道, 有一种叫Thibacillus Ferroxidans的细菌在氧气存在下,酸性溶液中,将黄铜矿氧化成硫酸盐:
4CuFeS2 + 2H2SO4 + 17O2 = 4CuSO4 + 2Fe2(SO4)3 + 2H2O
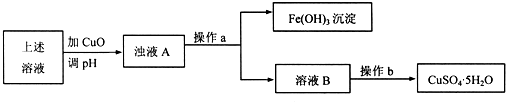
(1) 利用反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):
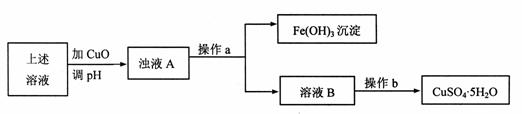
①溶液B显 (填“酸”、“碱”或“中”)性,原因是 (用离子方程式表示)。
②分析下表所提供的数据可知,加入CuO可除去CuSO4溶液中的Fe3+。
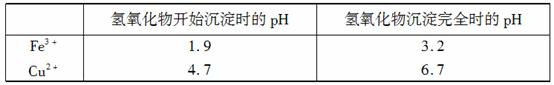
请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因:
③操作a的名称是 ,操作b的操作方法是 。
④检验溶液B中Fe3+是否被除尽的试剂是 ,证明Fe3+已被除尽的现象是 。
(2)在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方案只用一个反应来完成)。写出两种方案的化学方程式:
方案一:
方案二:
(1)①酸(1分) Cu2++2H2OCu(OH) 2+2H+ (2分)
②加入CuO使溶液中的c(H+)减小, c(OH-)浓度增大,使溶液中c (Fe3+)·c (OH-)3>Ksp[Fe(OH)3],使Fe3+生成沉淀而除去(2分)
③过滤(1分) 蒸发浓缩,冷却结晶(2分)
④KSCN溶液(1分) 溶液不变红(1分)
(2)CuSO4+Fe=FeSO4+Cu (2分)
2CuSO4+ 2H2O2Cu+O2↑+H2SO4(2分)

用黄铜矿炼铜按反应物和生成物可将总反应可以写成:
CuFeS2 + SiO2 + O2 → Cu + FeSiO3 + SO2
事实上冶炼反应是分步进行的。(1)黄铜矿在氧气作用下生成硫化亚铜和硫化亚铁;(2)硫化亚铁在氧气作用下生成氧化亚铁,并与二氧化硅反应生成矿渣;(3)硫化亚铜与氧气反应生成氧化亚铜;(4)硫化亚铜与氧化亚铜反应生成铜。
写出上述各个分步反应(1,2,3,4)的化学方程式。
2) 给出总反应方程式的系数。
3) 据最新报道, 有一种叫Thibacillus ferroxidans的细菌在氧气存在下可以将黄铜矿氧化成硫酸盐。反应是在酸性溶液中发生的。试写出配平的化学方程式。
4) 最近我国学者发现,以精CuFeS2矿为原料在沸腾炉中和O2 (空气)反应, 生成物冷却后经溶解、除铁、结晶,得到CuSO4·5H2O,成本降低了许多。实验结果如下:
| 沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 | |
| 生 成 物 | 水溶性Cu/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 酸溶性Cu/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 | |
| 酸溶性Fe/% | 8.56 | 6.72 | 3.46 | 2.78 | 2.37 | 2.28 | |
回答如下问题:
CuFeS2和O2主要反应的方程式为:
实际生产过程的沸腾炉温度为 600~620℃。控制反应温度的方法是:
温度高于600~620℃生成物中水溶性Cu (%)下降的原因是:
(19分) 用黄铜矿炼铜按反应物和生成物可将总反应可以写成:
CuFeS2 + SiO2 + O2 → Cu + FeSiO3 + SO2
事实上冶炼反应是分步进行的。(1)黄铜矿在氧气作用下生成硫化亚铜和硫化亚铁;(2)硫化亚铁在氧气作用下生成氧化亚铁,并与二氧化硅反应生成矿渣;(3)硫化亚铜与氧气反应生成氧化亚铜;(4)硫化亚铜与氧化亚铜反应生成铜。
1) 写出上述各个分步反应(1,2,3,4)的化学方程式。
2) 给出总反应方程式的系数。
3) 据最新报道, 有一种叫Thibacillus ferroxidans的细菌在氧气存在下可以将黄铜矿氧化成硫酸盐。反应是在酸性溶液中发生的。试写出配平的化学方程式。
4) 最近我国学者发现,以精CuFeS2矿为原料在沸腾炉中和O2 (空气)反应, 生成物冷却后经溶解、除铁、结晶,得到CuSO4?5H2O,成本降低了许多。实验结果如下:
沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 | |
生 成 物 | 水溶性Cu/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
酸溶性Cu/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 | |
酸溶性Fe/% | 8.56 | 6.72 | 3.46 | 2.78 | 2.37 | 2.28 | |
回答如下问题:
(1) CuFeS2和O2主要反应的方程式为:
(2) 实际生产过程的沸腾炉温度为 600~620℃。控制反应温度的方法是:
(3) 温度高于600~620℃生成物中水溶性Cu (%)下降的原因是: