题目内容
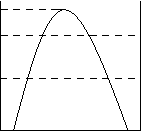
 A、B两种物质的饱和溶液的质量分数随温度变化的曲线如图.现分别在50gA和80gB中各加水150g加热溶解后并都蒸发掉水50g,冷却到t1℃,下列叙述正确的是
A、B两种物质的饱和溶液的质量分数随温度变化的曲线如图.现分别在50gA和80gB中各加水150g加热溶解后并都蒸发掉水50g,冷却到t1℃,下列叙述正确的是
- A.t1℃时溶液中A、B的质量分数相等
- B.t1℃时溶液中A的物质的量浓度等于B的物质的量浓度
- C.t1℃时析出固体B
- D.t1℃时两者均无固体析出
C
分析:根据题意,加水150克,加热溶解,同时蒸发掉50克水,冷却至T1℃,这一系列变化后,相当于在T1℃时用150g-50g=100g水分别去溶解50克A和80克B固体,判断此时的溶解情况;因此可根据饱和溶液的溶质质量分数随温度变化的曲线,算出T1℃两物质的溶解度,然后判断此时100g水所能溶解两种物质的最大值,从而对所做的判断进行评价.
解答:首先计算T1℃时A、B两物质的溶解度:根据饱和溶液的溶质质量分数随温度变化的曲线,T1℃时A、B两物质的饱和溶液的溶质质量分数相等都为40%,根据饱和溶液的溶质质量分数与溶解度的关系,可知此时两物质的溶解度相等,都为 ×100g≈67g;
×100g≈67g;
然后根据溶解度判断两物质在T1℃时的溶解情况:T1℃时A、B两物质的溶解度为67g,即此时100g水最多溶解A、B物质的质量都为67g,所以,加入的50gA可以全部溶解且形成不饱和溶液,加入的80gB不能全部溶解而成为饱和溶液;
综合以上分析,当降温到T1℃时固体A不会析出,而固体B物质析出80g-67g=13g;故A、B、D不正确,C正确;
故选C.
点评:本题考查溶液中溶质的质量分数及相关计算,解答本题时需要注意到所给出的曲线不是溶解度曲线而是饱和溶液的溶质质量分数随温度变化的曲线,可以使用饱和溶液中溶质质量分数与溶解度的关系进行数值转换.
分析:根据题意,加水150克,加热溶解,同时蒸发掉50克水,冷却至T1℃,这一系列变化后,相当于在T1℃时用150g-50g=100g水分别去溶解50克A和80克B固体,判断此时的溶解情况;因此可根据饱和溶液的溶质质量分数随温度变化的曲线,算出T1℃两物质的溶解度,然后判断此时100g水所能溶解两种物质的最大值,从而对所做的判断进行评价.
解答:首先计算T1℃时A、B两物质的溶解度:根据饱和溶液的溶质质量分数随温度变化的曲线,T1℃时A、B两物质的饱和溶液的溶质质量分数相等都为40%,根据饱和溶液的溶质质量分数与溶解度的关系,可知此时两物质的溶解度相等,都为
 ×100g≈67g;
×100g≈67g;然后根据溶解度判断两物质在T1℃时的溶解情况:T1℃时A、B两物质的溶解度为67g,即此时100g水最多溶解A、B物质的质量都为67g,所以,加入的50gA可以全部溶解且形成不饱和溶液,加入的80gB不能全部溶解而成为饱和溶液;
综合以上分析,当降温到T1℃时固体A不会析出,而固体B物质析出80g-67g=13g;故A、B、D不正确,C正确;
故选C.
点评:本题考查溶液中溶质的质量分数及相关计算,解答本题时需要注意到所给出的曲线不是溶解度曲线而是饱和溶液的溶质质量分数随温度变化的曲线,可以使用饱和溶液中溶质质量分数与溶解度的关系进行数值转换.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某种发动机燃料由A、B两种物质混合而成,A、B两种物质含有C、H、O三种元素的两种或三种。
已知常温下A、B及CO、H2的燃烧热如下:
1 mol物质 | A | B | CO | H2 |
燃烧热/kJ·mol-1 | 725 | 5518 | 283 | 286 |
A、B不同比例混合的燃料91.2 g,在足量的氧气中燃烧时,放出的热量Q与混合燃料中B的物质的量分数x的关系如下图。(计算过程中保留两位小数)
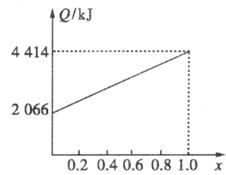
(1)相对分子质量A为_________,B为_________。
(2)73 g由A、B等物质的量混合而成的燃料在160 LO2中完全燃烧后,冷却后得到104 L气体,通过碱石灰充分吸收后剩余3.2 L(气体体积均在标准状况下测定)。由此可求得混合物中n(C):n(H):n(O)=_________,若A是醇,B为饱和烃,则A的分子式为_________,B分子式为_________。
(3)l mol由A、B等物质的量混合而成的燃料在一定量的氧气中燃烧,放出热量2 980 kJ,则反应中生成CO_________mol。